Základní metabolické cesty sacharidů v buňce
Primárním úlohou základních metabolických cest je zpracování látek z potravy. Z procesu trávení získává organismus tři základní monosacharidy (glukosu, fruktosu a galaktosu), z nichž glukosa při běžné stravě výrazně převažuje. Glukosa je v organismu přeměňována několika metabolickými cestami (Obr. 2). Štěpením glukosy v glykolýze získává buňka energii. U člověka probíhá ve svalech při intenzivní svalové práci, kdy přísun kyslíku nestačí pokrýt potřebu aerobní degradace živin, anaerobní glykolýza, jejímž produktem je laktát. Za aerobních podmínek navazuje na glykolýzu citrátový cyklus a dýchací řetězec s oxidační fosforylací. Spojením těchto drah je glukosa úplně oxidována až na vodu a CO2 za vzniku ATP. Alternativou glykolýzy a citrátového cyklu je pentosový cyklus, což je katabolický děj, jehož smyslem je tvorba pentos (ribosa pro syntézu nukleových kyselin) a redukovaného NADPH. Pokud se do organismu dostává větší množství glukosy, než se může aktuálně využít, vytváří si organismus energeticky využitelné rezervy. Z glukosy se tak v játrech a svalech syntetizuje zásobní polysacharid glykogen, jinou cestou se z acetyl-CoA vzniklého z oxidace glukosy syntetizují v tukové tkáni mastné kyseliny a TAG (lipogeneze). Pokud je okamžitá potřeba energie větší, dochází k degradaci glykogenu. V játrech při ní vzniká glukosa, která je uvolněna do krve a transportována do periferních tkání. Ve svalech pak vzniká glukosa-6-fosfát, který se zapojuje do glykolýzy. Pokud nemá organismus dostatečný přísun živin ani energetické rezervy, využívá k syntéze glukosy některé nízkomolekulární necukerné látky (např. laktát, alanin, glukogenní aminokyseliny, glycerol). Tento proces se nazývá glukoneogeneze. Necukerné látky pro syntézu glukosy jsou do jater dodávány ze svalů a červených krvinek v rámci Coriho cyklu a glukoso-alaninového cyklu. Využití glukosy jednotlivými tkáněmi je popsáno v předchozí kapitole.
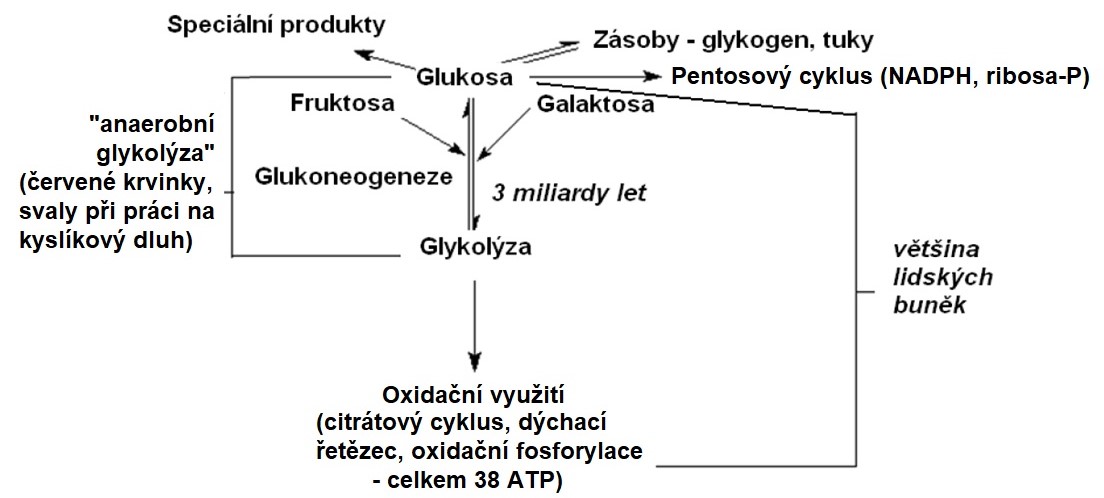
Obr. 2. Přehled metabolických cest glukosy.
Monosacharidy se zapojují do metabolismu prostřednictvím fosforylace, která je katalyzována kinasami za účasti ATP. Strukturní rozdíly mezi jednotlivými monosacharidy určují, který enzym zahájí jeho metabolizaci. Glukosa může být fosforylována hexokinasou nebo glukokinasou. Rozdíly mezi těmito enzymy jsou shrnuty v předchozí kapitole. V játrech se nacházejí fruktokinasa a galaktokinasa, kinasy specifické pro fruktosu a galaktosu a jejich aktivita není ovlivněna hladověním ani insulinem. Jedná se o enzymy s vysokou afinitou k těmto monosacharidům, jejichž působením vzniká fruktosa‑1-fosfát a galaktosa-1-fosfát. Hexokinasa je kromě glukosy schopná metabolizovat s výrazně menší afinitou i fruktosu a mannosu. Galaktosa pravděpodobně není tímto enzymem fosforylována.
Metabolismus glykogenu
Glykogen je zásobním polysacharidem živočichů (svaly, játra) se strukturou větvené levotočivé šroubovice složené z glukosových jednotek. Monomery glykosy jsou v každé větvi spojeny glykosidickými vazbami α(1→4) a další větve jsou připojeny vazbou α(1→6). Celá struktura drží pohromadě pomocí kotvícího proteinu glykogeninu.
Syntéza glykogenu vychází z UDP-glukosy. K jejímu vzniku je nejprve třeba přeměnit glukosa-6-fosfát fosfoglukomutasou na glukosa-1-fosfát, který je za účasti UTP aktivován působením UDP‑glukosadifosforylasy na UDP-glukosu. První krátký úsek glykogenu syntetizuje glykogenin, který autokatalyticky připojuje první UDP-glukosu na hydroxylovou skupinu tyrosinu v pozici 194 a dalších sedm připojuje již glykosidickou vazbou. Vzniká tak glykogenprimer. Poté přebírá aktivitu glykogensynthasa, která připojuje další glukosové jednotky vazbou α(1→4). Rozvětvená struktura glykogenu je pak výsledkem působení větvícího enzymu (amylo(1,4→1,6)transglykosylasa; „branching enzyme“), který z řetězce o minimální délce 11 jednotek přenese šest jednotek na jiný řetězec a připojí je vazbou α(1→6).
Degradace glykogenu je katalyzována glykogenfosforylasou, která odštěpuje z glykogenu jednotlivé glukosové jednotky ve formě glukosa-1-fosfátu. Glykogenfosforylasa je schopná štěpit pouze vazby α(1→4) a její činnost končí zhruba čtyři jednotky od větvení. Pak nastupuje odvětvující enzym (amylo-α(1→6)glukosidasa), který přenese tři glukosové jednotky na sousední řetězec, kde je připojí vazbou α(1→4). Poslední glukosová jednotka je tímto enzymem odštěpena a uvolněna jako glukosa. Vznikající glukosa-1-fosfát je fosfoglukomutasou přeměněn na glukosa-6-fosfát, který se může zapojit do glykolýzy (svaly), nebo z něj glukosa-6-fosfatasa odštěpí fosfátovou skupinu a vzniklá glukosa je uvolněna do krevního oběhu (játra, ledviny).
Regulace syntézy a degradace glykogenu probíhá prostřednictvím allosterické regulace a kovalentní modifikace (reverzibilní fosforylace a defosforylace enzymu) glykogensythasy a glykogenfosforylasy. Aktivní forma těchto enzymů se označuje písmenem „a“ (tj. glykogensynthasa a, glykogenfosforylasa a), zatímco neaktivní forma je označena písmenem „b“ (tj. glykogensynthasa b, glykogenfosforylasa b). Fosforylace se zvyšuje v reakci na tvorbu cAMP, která je katalyzovaná adenylátcyklasou. K aktivaci adenylátcyklasy dochází působením hormonů glukagonu a adrenalinu (Obr. 3). cAMP je hydrolyzován fosfodiesterasou, jejíž aktivita je v játrech aktivována insulinem (Obr. 4). Regulace glykogensynthasy a glykogenfosforylasy je protichůdná – ve stejnou dobu, kdy je glykogenfosforylasa aktivována vzestupem cAMP, je glykogensynthasa přeměněna na neaktivní formu. Inhibice syntézy glykogenu tak zesiluje glykogenolýzu a inhibice rozkladu glykogenu zesiluje výslednou glykogenezi.
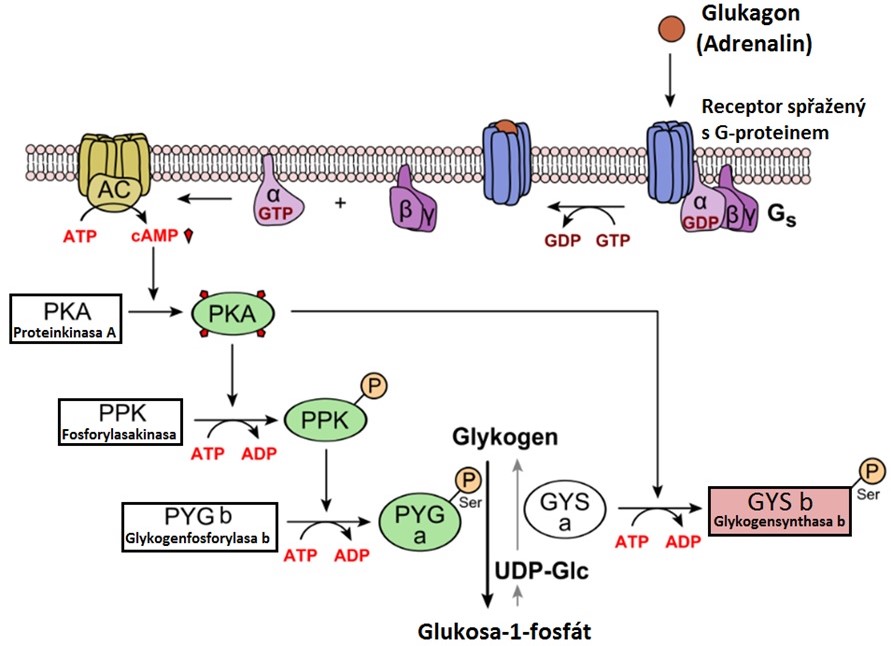
Obr. 3. Regulace metabolismu glykogenu glukagonem a adrenalinem (upraveno z Wikimedia Commons 1).
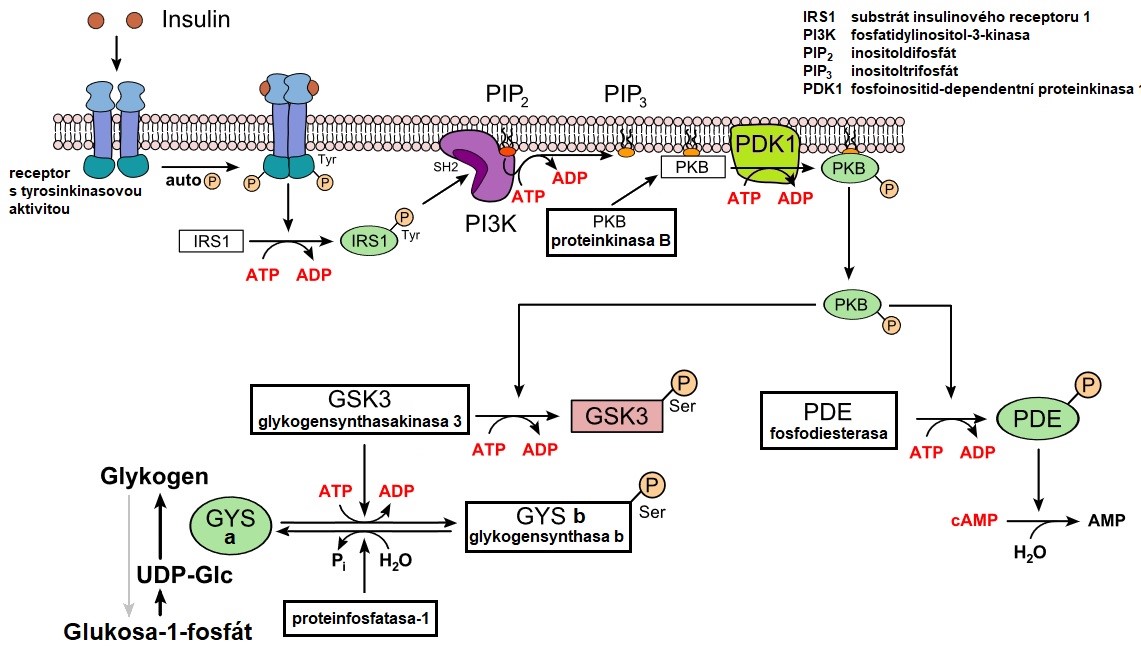
Obr. 4. Regulace metabolismu glykogenu insulinem (upraveno z Wikimedia Commons 2).
Metabolismus fruktosy
Hlavním zdrojem volné fruktosy v potravě je ovoce a med, dále vzniká ve střevě štěpením sacharosy. Protože fruktosa tvoří při současném složení potravy (slazení sacharózou a fruktosovým sirupem, umělá sladidla) až čtvrtinu všech přijatých sacharidů, není její metabolismus zcela zanedbatelný. Nadměrný příjem fruktosy ve sladkých nápojích přispívá k růstu prevalence obezity a to zejména u dětí a mladistvých.
Fruktosa přijatá potravou je metabolizována zejména v játrech. Její metabolismus v hepatocytu je rychlejší než metabolismus glukosy jednak díky snadnému transportu přes membránu a také díky tomu, že obchází regulační krok katalyzovaný fosfofruktokinasou. Fruktokinasa, která je přítomná v játrech, ledvinách a ve střevě, katalyzuje fosforylaci fruktosy na fruktosa-1-fosfát. Ten je štěpen na D-glyceraldehyd a dihydroxyacetonfosfát jaterním enzymem aldolasou B. Tento enzym v játrech působí v glykolýze, kde štěpí rovněž fruktosa-1,6-bisfosfát (v ostatních tkáních plní tuto funkci aldolasa A). D-glyceraldehyd je triokinasou fosforylován na glyceraldehyd-3-fosfát, který vstupuje do glykolýzy. Po příjmu stravy bohaté na fruktosu či sacharosu dochází vlivem jejího rychlého metabolismu k rychlé spotřebě ATP, která je provázena zvýšenou tvorbou AMP, inosinmonofosfátu a kyseliny močové. Dále dochází ke zvýšené syntéze mastných kyselin, jejich esterifikaci, syntéze lipoproteinů a jejich sekreci ve formě VLDL do krevního oběhu, což může vyvolat zvýšení koncentrace TAG v krvi a v konečném důsledku zvýšení LDL-cholesterolu. V mimojaterních tkáních je fruktosa fosforylována hexokinasou na fruktosa-6-fosfát, který se zapojuje do glykolýzy. Glukosa však fosforylaci fruktosy inhibuje, protože je pro hexokinasu lepším substrátem. Přesto může být fruktosa metabolizována v kosterním svalstvu a v tukové tkáni.
Metabolismus galaktosy
Galaktosa pochází z hydrolýzy mléčného cukru laktosy. V organismu se využívá k syntéze laktosy v období kojení, kdy v reakci katalyzované laktosasynthasou dochází ke kondenzaci UDP-galaktosy s glukosou. Je rovněž součástí glykolipidů (cerebrosidů), glykoproteinů a proteoglykanů. V játrech se snadno přeměňuje na glukosu. Fosforylaci galaktosy katalyzuje galaktokinasa za účasti ATP, vznikající galaktosa-1-fosfát reaguje s UDP-glukosou za vzniku UDP-galaktosy a glukosa-1-fosfátu. Tato reakce je katalyzována galaktosa-1-fosfáturidyltransferasou. UDP-galaktosa je pak UDP‑galaktosa-4-epimerasou přeměněna na UDP-glukosu. Tato reakce zahrnuje oxidaci a poté redukci na uhlíku 4 za účasti NAD+. Vznikající UDP-glukosa je pak využita k syntéze glykogenu. Epimerasová reakce je vratná, takže glukosa může být přeměněna na galaktosu a příjem galaktosy potravou tedy není nezbytný.