Homeostáza glukosy
Koncentrace glukosy v krvi (glykemie) je za fyziologických podmínek udržována v rozmezí 3,9-5,6 mmol/l nalačno a nižší než 10 mmol/l po jídle. Glykemie je výsledkem příjmu, syntézy, přeměny, spotřeby a ztrát glukosy (Obr. 5). Pro některé tkáně, jako jsou mozek a erytrocyty, je glukosa za normálních podmínek jediným zdrojem energie. Zároveň nedochází k poškození orgánů, které vyvolává dlouhodobé působení vysokých koncentrací glukosy (viz. chronické komplikace diabetu mellitu). Z těchto důvodů je udržení stálé koncentrace glukosy v krvi jedním ze základních cílů regulačních mechanismů, uplatňujících se v distribuci a metabolismu glukosy. Glykemie je regulována hormonálně (např. insulin, glukagon, adrenalin, kortisol) a nervově (působení parasympatiku, sympatiku a hypothalamu).
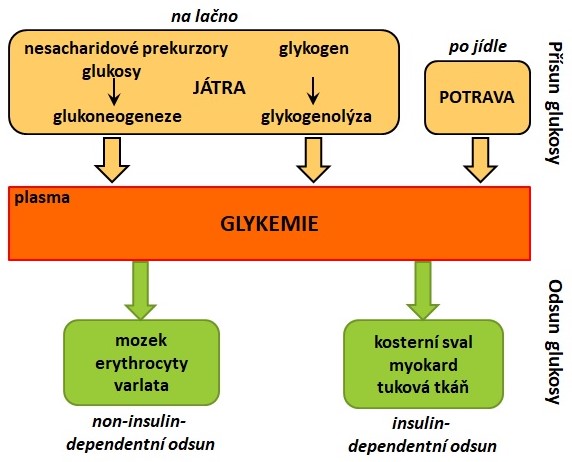
Obr. 5. Homeostáza glukosy (upraveno z Vejražka 2010).
Fáze homeostázy glukosy
Proces, který reguluje metabolismus glukosy a pomáhá udržovat její stálou hladinu v plasmě, se nazývá homeostáza glukosy. Z pokusů na obézních pacientech, kteří z terapeutických důvodů podstupovali dlouhodobé hladovění za účelem redukce hmotnosti, byly odvozeny fáze homeostázy glukosy a procesy, které se podílejí na udržení stálé glykemie. Homeostázu glukosy lze rozdělit do pěti fází (Obr. 6). První fáze je stavem nasycenosti, kdy jsou zdrojem glukosy sacharidy z potravy. Druhá fáze nastává ve chvíli, kdy je první zdroj glukosy vyčerpán a glykemie je udržována díky degradaci jaterního glykogenu. Jak se tento zdroj glukosy postupně zmenšuje, tak se začíná postupně nabývat na významu jaterní glukoneogeneze z laktátu, glycerolu a alaninu. Ta je hlavním zdrojem glukosy ve třetí fázi homeostázy. Všechny tyto změny proběhnou během prvních zhruba 20 hodin hladovění v závislosti na zásobách glykogenu, fyzické aktivitě a míře nasycení jedince. Po několika dnech hladovění se organismus přesouvá do čtvrté fáze, ve které závislost na glukoneogenezi postupně klesá. Nahromaděné ketolátky dosahují koncentrací, které jsou dostatečně vysoké na to, aby vstoupily do mozku a mohly pokrýt část jeho energetických potřeb. Na významu v této fázi nabývá renální glukoneogeneze. Pátá fáze nastává u extrémně obézních jedinců při dlouhodobém hladovění a je charakterizována ještě menší závislostí na glukoneogenezi. Energetické požadavky většiny tkání jsou do značné míry uspokojeny oxidací mastných kyselin nebo ketolátek. Dokud jsou koncentrace ketolátek vysoké, je proteolýza omezena a svalové proteiny a enzymy jsou ušetřeny. Po spotřebování veškerého tuku se začnou rozkládat svalové proteiny a po jejich degradaci následuje smrt jedince.

Obr. 6. Fáze homeostázy glukosy (upraveno z Devlin 1997)
Regulace glykemie
Zásadní význam v regulaci metabolismu glukosy a udržení stálé glykemie má hypothalamus (centra hladu a sytosti). Zvýšení glykemie je jedním ze signálů pro navození pocitu sytosti, zatímco při snížení hladiny glukosy zprostředkují tato centra pocit hladu. Vzhledem k tomu, že běžná strava obsahuje zejména sacharidy, lze tento způsob regulace považovat za základní mechanismus, který umožňuje dlouhodobě udržet stálou hladinu glykemie i zásoby glykogenu a triacylglycerolů (TAG). Hypothalamus má zároveň vliv na tonus autonomního nervového systému a tvorbu celé řady hormonů, které přímo ovlivňují metabolismus sacharidů (např. insulin, glukagon, kortisol, adrenalin). Regulace glykemie prostřednictvím insulinu a glukagonu je shrnuta v Obr. 7. Vliv jednotlivých hormonů na hladinu glukosy je uveden v Tabulce 2.
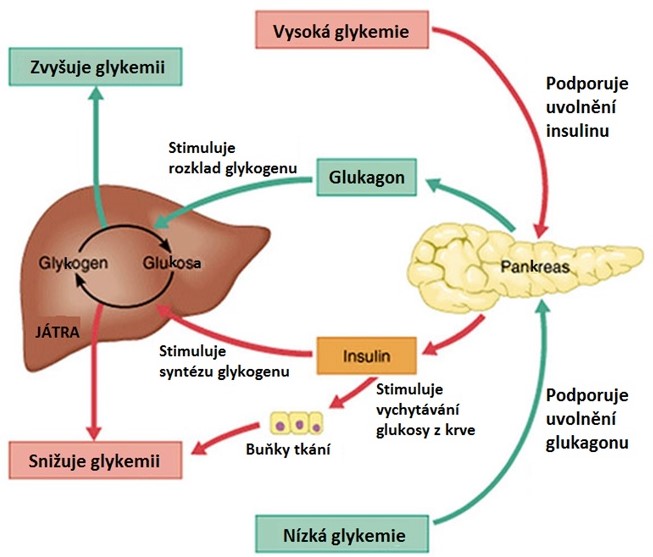
Obr. 7. Regulace glykemie prostřednictvím insulinu a glukagonu (upraveno z Marieb 2001)
Tabulka 2. Vliv hormonů na glykemii, podnět pro vyplavení a mechanismus jejich účinku
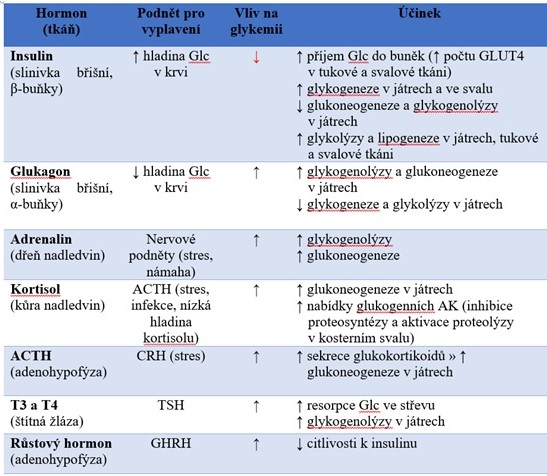
Glc, glukosa; ACTH, adrenokortikotropní hormon; AK, aminokyseliny; CRH, kortikoliberin; TSH, thyreotropin hormon; GHRH, somatoliberin
Hormonální regulace glykemie
V regulaci glykemie se kromě substrátů, produktů, vzdálenějších metabolitů, kofaktorů a dalších látek uplatňují především hormony.
Insulin
Insulin je hlavním anabolickým hormonem organismu. Jedná se o proteohormon produkovaný β-buňkami Langerhansových ostrůvků pankreatu. Je tvořen řetězcem A (21 aminokyselin) a řetězcem B (30 aminokyselin) spojených dvěma disulfidovými můstky, další můstek spojuje dva cysteinové zbytky v řetězci A. Transkripcí a translací genu INS vzniká peptid preproinsulin (110 aminokyselin), z jehož struktury je v endoplasmatickém retikulu signální peptidasou odstraněn signální peptid. Vzniklý proinsulin (86 aminokyselin) je zabalen do váčků Golgiho aparátu, kde se podrobuje tvorbě disulfidických vazeb a částečné proteolýze. Výsledkem je vznik aktivního insulinu a C-peptidu, které se společně vylučují do krevního oběhu ze sekrečních granul (váčky).
Sekrece insulinu je spuštěna stoupající hladinou glykemie (též aminokyseliny Arg a Leu a mastné kyseliny). Do β-buněk pankreatu je při hyperglykemii ve větší míře transportérem GLUT2 transportován glukosa, která je fosforylována glukokinasou. Stoupající hladina glukosy v krvi zvyšuje metabolický tok glykolýzou a citrátovým cyklem a tím dochází ke zvýšení produkce ATP, který pak inhibuje ATP-sensitivní K+-kanály. V důsledku této inhibice stoupá intracelulárním koncentrace K+, což vyvolá depolarizaci plasmatické membrány s následným otevřením napěťově-řízených Ca2+‑kanálů. Stoupající intracelulární koncentrace Ca2+ stimuluje exocytosu sekrečních granul a tedy i uvolnění insulinu (Obr. 8).
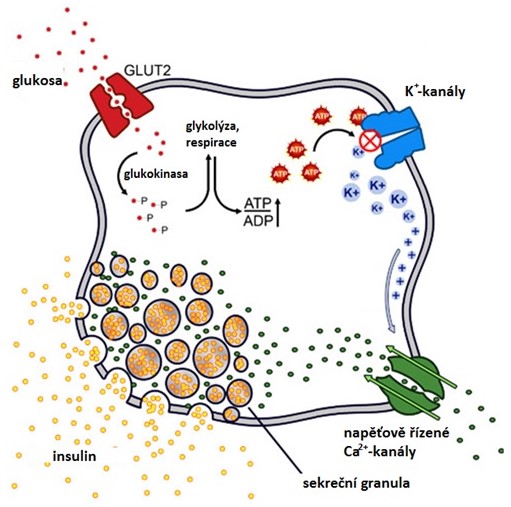
Obr. 8. Sekrece insulinu (upraveno z Rao et al. 2015)
Na plasmatické membráně cílových buněk je přítomný insulinový receptor, který přenáší signál do nitra buňky. Jedná se heterotetramer složený ze dvou α a dvou β řetězců spojených disulfidovými vazbami. Řetězec α je extracelulární a zajišťuje vazbu insulinu, zatímco řetězec β je transmembránový a jeho intracelulární doména má tyrosinkinasovou aktivitu. Po vazbě insulinu na receptor dojde k oligomerizaci receptorů a konformační změně jejich molekul, jejímž důsledkem je autofosforylace intracelulárních částí sousedních polovin receptoru. K převodu signálu do buňky slouží adaptorové proteiny, v tomto případě tzv. substráty insulinového receptoru (IRS-1 až IRS-6), které jsou fosforylovány aktivovaným receptorem. Pro řízení kaskády dalších intracelulárních reakcí jsou klíčové IRS-1 a IRS-2, které vyvolávají aktivaci fosfatidylinositol-3-kinasy (PI3K) a mitogenem-aktivované kinasy (MAPK) a vystavení transportérů GLUT4 na plasmatické membráně buněk. Výsledkem aktivace insulinového receptoru je transport glukosy do buňky (GLUT4), metabolické účinky insulinu podporující syntézu proteinů, lipidů a glykogenu a růstové účinky tohoto hormonu (Obr. 9).
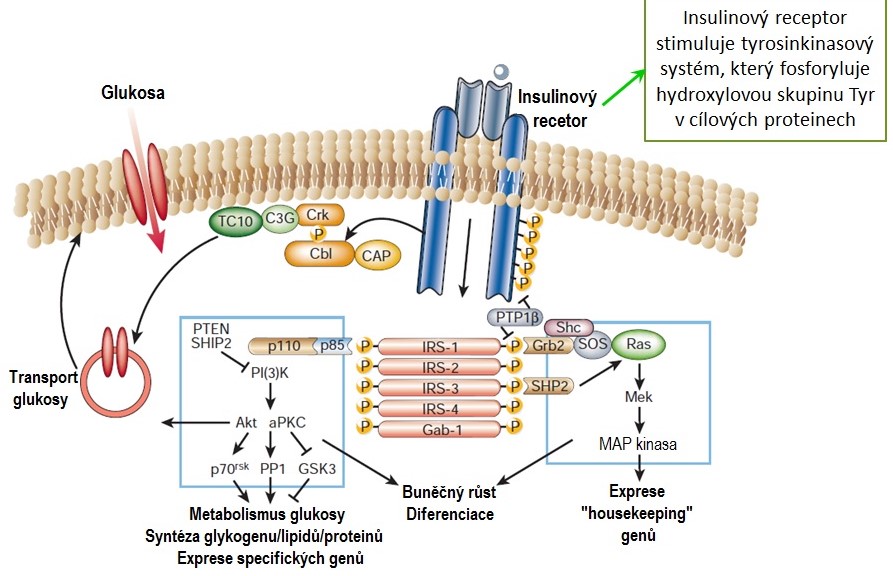
Obr. 9. Insulinový receptor a přenos signálu (upraveno z Saltiel a Kahn 2001)
Hypoglykemizující účinek insulinu se uskutečňuje několika mechanismy:
V játrech insulin indukuje syntézu glukokinasy a dalších klíčových enzymů glykolýzy (fosfofruktokinasa, pyruvátkinasa) a aktivuje pyruvátdehydrogenasový komplex. Dochází k inhibici účinků hormonů, které působí přes cAMP, jejímž výsledkem je potlačení glukoneogeneze a glykogenolýzy. Dochází k útlumu syntézy klíčových enzymů glukoneogeneze (pyruvátkarboxylasa, fosfoenolpyruvátkarboxykinasa, fruktosa-1,6-bisfosfatasa, glukosa-6-fosfatasa). Díky antilipolytickému účinku insulinu (inhibice hormon-sensitivní lipasy) je utlumena syntéza ketolátek. Insulin podporuje syntézu proteinů na úrovni ribosomů a tlumí proteolýzu.
V kosterním svalstvu stoupá působením insulinu transport glukosy do buněk (přenos GLUT4 do plasmatické membrány). Je aktivována syntéza glykogenu díky zvýšené nabídce substrátu a díky stimulaci přeměny inaktivní glykogensynthasy na aktivní formu. Insulin stimuluje glykolýzu (zvýšená nabídka substrátu, aktivace fosfofruktokinasy) a oxidační dekarboxylaci pyruvátu (přeměna neaktivní pyruvátdehydrogenasy na aktivní formu). Zvyšuje se příjem mastných kyselin a jejich přeměna na TAG. Rovněž je podporován příjem aminokyselin buňkou (insulin stimuluje aktivní transport) a proteosyntéza, proteolýza je potlačena.
V tukové tkáni vyvolává insulin zvýšení transportu glukosy do buněk (GLUT4), stimulaci glykolýzy a oxidační dekarboxylace pyruvátu (jako ve svalech). Díky aktivaci acetyl-CoA-karboxylasy insulinem se zvyšuje tvorba mastných kyselin a tedy i spotřeba NADPH. Oxidovaný koenzym NADP+ je ve zvýšené míře nabízen pro oxidaci glukosy v pentosovém cyklu, jehož aktivita stoupá. Inhibicí hormon-sensitivní lipasy vyvolává zastavení lipolýzy.
K hypoglykemizujícímu účinku insulinu přispívají i další látky – amylin a inkretiny. Amylin je komplementární faktor insulinu, který je rovněž syntetizován v β-buňkách pankreatu a je z nich uvolněn spolu s insulinem. Jedná se o neuroendokrinní hormon s receptory v CNS. Výsledkem jeho působení je snížení postprandiální sekrece glukagonu, zpomalení vyprazdňování žaludku a tedy oddálení vstupu živin do cirkulace, snížení příjmu potravy a zlepšení glukosového metabolismu. Celkovým účinkem amylinu je zpomalení vstupu glukosy do cirkulace a tedy i snížení vzestupu postprandiální glykemie. Analoga amylinu (pramlintid) patří mezi antidiabetika používaná k léčbě diabetu mellitu 1. i 2. typu. Inkretiny GLP-1 (glucagon-like peptide-1) a GIP (glucose-dependent insulinotropic peptide) jsou peptidové hormony uvolňované z L-buněk tenkého střeva po jídle. Inkretinový efekt byl popsán již v 60. letech 20. století, kdy bylo zjištěno, že p.o. podání glukosy způsobí až dvojnásobně větší uvolnění insulinu z pankreatu než podání parenterální (i.v. nebo i.p.). Inkretiny tedy zvyšují sekreci insulinu po jídle ještě před vzestupem glykemie, dále inhibují sekreci glukagonu, zpomalují vyprazdňování žaludku a navozují pocit sytosti. Inaktivace těchto hormonů je zprostředkována dipeptidylpeptidasou-4 (DPP-4), která je degraduje. Na využití inkretinového systému jsou založeny dva léčebné přístupy v terapii diabetes mellitus (DM), protože u diabetiků 2. typu byla popsána dysfunkce tohoto systému. Podávají se jednak inhibitory DPP-4 označované jako gliptiny (např. sitagliptin, vildagliptin), které prodlužují biologický poločas endogenních inkretinů, nebo se podávají inkretinová mimetika (např. exenatid, liraglutid), která aktivují receptor pro GLP-1 a jsou odolná vůči působení DPP-4.
Jestliže insulin považujeme za faktor vyvolávající hypoglykemii, má v tomto směru mezi hormony několik antagonistů, jejichž působením vzniká hyperglykemie:
Glukagon
Glukagon je polypeptid (29 aminokyselin) produkovaný α-buňkami Langerhansových ostrůvků pankreatu. Jeho sekrece je stimulována především hypoglykemií, ale také sníženou koncentrací mastných kyselin a glukogenních aminokyselin, katecholaminy, gastrinem a pankreozyminem. Tento hormon se na membránách hepatocytů a adipocytů váže na receptor spřažený s G-proteinem, jehož aktivace stimuluje adenylátcyklasu produkující cAMP. Zvýšená hladina cAMP aktivuje proteinkinasu A, která fosforyluje cílové enzymy a tím mění jejich aktivity.
K hlavním účinkům glukagonu patří aktivace glykogenolýzy (aktivace glykogenfosforylasy) a inhibice syntézy glykogenu (inhibice glykogensynthasy) fosforylací klíčových enzymů těchto drah. Dále je stimulována proteolýza v játrech a využití aminokyselin v glukoneogenezi. V tukové tkáni je cestou cAMP aktivována hormon-sensitivní lipasa a tím i lipolýza. Výsledkem působení glukagonu je zejména vzestup glykemie.
Adrenalin
Adrenalin (Obr. 10) je derivátem aminokyseliny tyrosinu a je syntetizován v buňkách dřeně nadledvin. Jedná se o stresový hormon, který je do krve vyplavován na impulsy preganglionálních sympatických neuronů inervujících dřeň nadledvin. Cílem adrenalinu je mobilizace organismu pro zátěžovou situaci. Své účinky realizuje prostřednictvím vazby na α- a β-adrenoreceptory. Metabolické působení adrenalinu se realizuje zejména prostřednictvím β‑receptorů cestou cAMP (aktivace adenylátcyklasy), vazbou na α-receptory vyvolá adrenalin zvýšení intracelulární koncentrace Ca2+. Takto vyvolává adrenalin změnu aktivity enzymů metabolismu sacharidů a lipidů.
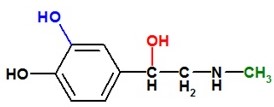
Obr. 10. Adrenalin
Mezi hlavní účinky adrenalinu patří aktivace glykogenfosforylasy kovalentní modulací (fosforylací). Tento princip aktivace je stejný jako v případě glukagonu, ale účinek glukagonu je soustředěn na jaterní buňky, zatímco adrenalin působí kromě jater (kde je jeho účinek méně významný) hlavně v kosterním svalstvu. Inaktivace glykogensynthasy adrenalinem se uskutečňuje především ve svalech a dále v játrech (mechanismus obdobný jako u glukagonu). Adrenalin aktivuje hormon-sensitivní lipasu v tukové tkáni. Kromě účinků na regulatorní enzymy vyvolává adrenalin také zvýšení sekrece glukagonu a snížení sekrece insulinu.
Glukokortikoidy (kortisol)
Tyto steroidní hormony jsou produkovány kůrou nadledvin (zona fasciculata) a jejich hlavním představitelem je kortisol (Obr. 11). Jedná se o lipofilní látky, které procházejí membránou do cytoplasmy, kde se váží na receptor pro glukokortikoidy a společně se pak přesouvají do jádra buňky, kde po vazbě na responzivní elementy DNA ovlivňují transkripci cílových genů.
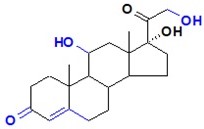
Obr. 11. Kortisol
Metabolické účinky glukokortikoidů jsou rozsáhlé. Celkově se jejich působení projevuje zvýšením koncentrace glukosy, mastných kyselin a aminokyselin v krvi. V metabolismu sacharidů se nejvýrazněji projevuje aktivace jaterní glukoneogeneze zvýšením syntézy klíčových enzymů (pyruvátkarboxylasa, fosfoenolpyruvátkarboxykinasa, fruktosa-1,6-bisfosfatasa, glukosa-6-fosfatasa). V tukové tkáni zvyšují glukokortikoidy lipolýzu, ve svalech a dalších periferních tkáních snižují syntézu proteinů a zvyšují proteolýzu.
Hormony štítné žlázy
Thyroxin a trijodtyronin (Obr. 12) jsou jodované deriváty aminokyseliny tyrosinu, které jsou syntetizované ve folikulárních buňkách štítné žlázy. Jedná se o lipofilní hormony, které se v cílových buňkách váží na intracelulární receptory a v jádře pak ovlivňují transkripci cílových genů.
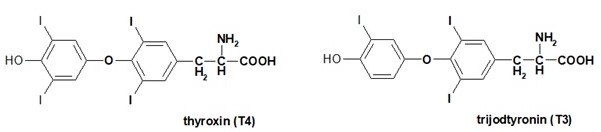
Obr. 12. Thyroxin a trijodtyronin
Tyto hormony mají především metabolický a kalorigenní účinek – zvyšují celkový metabolismus, počet a velikost mitochondrií, spotřebu kyslíku, tvorbu tepla a výdej energie. Zvyšují absorpci sacharidů za střeva a stimulují oxidaci glukosy v periferních tkáních. Aktivují glukoneogenezi v játrech a degradaci glykogenu, takže jejich celkový účinek je hyperglykemizující. Stimulují lipolýzu a díky snížení syntézy a zvýšenému vylučování žlučí snižují celkovou hladinu cholesterolu v krvi. Účinek thyreoidálních hormonů na metabolismus proteinů je komplexní – u některých enzymů stimulují jejich syntézu (např. enzymů dýchacího řetězce, Na+/K+‑ATPasy), zatímco u jiných podporují jejich degradaci (např. rozklad svalových proteinů). Dále zvyšují expresi růstového hormonu a zesilují účinky katecholaminů tím, že zvyšují počet adrenergních receptorů.
Kortikotropin (ACTH)
Tento polypeptid (39 aminokyselin) produkovaný adenohypofýzou působí jako antagonista insulinu nepřímo. Je vyplavován při stresových situacích (stimulace sekrece hypothalamickým kortikoliberinem), jeho cílovou tkání je kůra nadledvin, kde zvyšuje tvorbu a sekreci glukokortikoidů. Kromě toho aktivuje hormon-sensitivní lipasu a tím stimuluje lipolýzu a uvolnění mastných kyselin z tukových zásob.
Růstový hormon (somatotropin)
Jedná se o proteohormon (191 aminokyselin) produkovaný adenohypofýzou, jehož metabolické účinky se projevují celkovou podporou anabolismu. Inhibuje vstup glukosy do buněk a glykolýzu, v tomto směru má antiinsulinový účinek. V adipocytech stimuluje lipolýzu, uvolněné mastné kyseliny jsou oxidovány. Transport aminokyselin do buněk je, na rozdíl od transportu glukosy, somatotropinem stimulován a stoupá proteosyntéza.
Regulace glykemie ledvinami
Glukosa je z plasmy filtrována v ledvinách do primární moči, kde její koncentrace v relaci s glykemií. Z primární moči se aktivním transportem (transportér SGLT2) resorbuje v proximálních tubulech, čímž se organismus chrání před ztrátami tohoto cenného zdroje energie. Proto disponují proximální tubuly značnou rezervní kapacitu (za fyziologického stavu jsou vytíženy zhruba z jedné třetiny). Při hyperglykemii je tento transportní systém více vytížen, a pokud překročí koncentrace glukosy hodnoty kolem 10 mmol/l, je kapacita transportního systému překročena, transportéry jsou nasyceny (tzv. ledvinný práh) a glukosa se objevuje v moči (glykosurie). Glykosurie je nejčastějším nálezem vedoucím k odhalení DM, avšak nepřítomnost glukosy v moči tuto diagnosu nevylučuje.
Při renální glykosurii, která vzniká na podkladě tubulárních dysfunkcí (např. mutací genu kódujícího transportér SGLT2), přechází glukosa do moči i při fyziologických hladinách glykemie. Jedná se o relativní benigní onemocnění, které nemá souvislost s případným vznikem DM.
Regulace metabolismu glukosy ve stavu nasycení a ve stavu lačnění
Regulace glykemie se liší ve stavu nasycení a ve stavu lačnění. Obecně lze říci, že ve stavu nasycení (anabolický stav) je aktivován vstup glukosy do buněk, glykolýza a glykogenogeneze. Ve stavu lačnění (katabolické stavy – např. hladovění, fyzická zátěž, stres) jsou naopak aktivovány mechanismy, které umožní uvolnit glukosu z jater do krve, glykogenolýza a glukoneogeneze. Metabolismus glukosy je v jednotlivých tkáních díky jejich odlišné enzymové výbavě a citlivosti k působení hormonů ovlivněn různým způsobem.
Stav nasycení
Po příjmu potravy bohaté na sacharidy stoupá hladina glukosy a aktivují se mechanismy, které umožní její vstup do buněk a následné využití (syntéza glykogenu a TAG). Glukosa prostupuje do krevního oběhu přímo přes epiteliální buňky střeva a portální žilou vstupují do jater. Vzestup glykemie způsobí vyplavení insulinu z β-buněk pankreatu a snížení koncentrace glukagonu v tělních tekutinách. Insulin vyvolá zvýšení počtu GLUT4 v plasmatických membránách buněk kosterního svalu a adipocytů, a tak usnadní odstranění glukosy z krevního oběhu. Díky zvýšení poměru insulin/glukagon dojde k aktivaci drah, které zpracovávají glukosu (glykolýza, syntéza glykogenu), a je tak udržován koncentrační gradient glukosy mezi intra- a extracelulárním prostředím. Tento gradient je nezbytný pro vstup glukosy do hepatocytů.
V játrech je glukosa přeměněna na glykogen, na pyruvát a laktát (glykolýza) nebo použita v pentosovém cyklu k tvorbě NADPH pro syntetické pochody. Pyruvát je oxidován na acetyl-CoA, který může být použit k syntéze TAG, nebo oxidován až na CO2 a H2O v citrátovém cyklu. Určité množství glukosy unikne do dalších tkání. Mozek a varlata jsou prakticky úplně závislé na glukose jako zdroji ATP. Dalším významným uživatelem glukosy jsou erytrocyty a dřeň ledvin, které dokáží glukosu přeměnit pouze na pyruvát a laktát, a tuková tkáň, která ji přemění na TAG. Svalové buňky syntetizují z glukosy glykogen nebo ji metabolizují v glykolýze a citrátovém cyklu. Laktát a pyruvát vytvořené periferními tkáněmi jsou vychytány v játrech a přeměněny na TAG (lipogeneze). Ve stavu nasycení játra zpracovávají glukosu a glukoneogeneze je potlačena, takže Coriho cyklus je přerušen (Obr. 13).
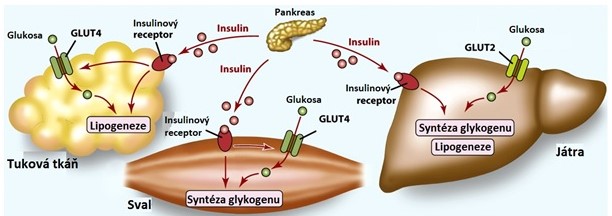
Obr. 13. Hormonální regulace metabolismu glukosy ve stavu nasycení (upraveno z Corkill 2017)
Stav lačnění, hladovění a fyzická zátěž
V mezidobí mezi jednotlivými jídly je třeba doplňovat hladinu glukosy z endogenních zdrojů. Játra jsou jediným orgánem, který je schopen do krevního oběhu dodávat dostatečné množství glukosy, protože jsou vybavena zásobou glukosy ve formě glykogenu i všemi enzymy glukoneogeneze, včetně glukosa-6-fosfatasy.
Během lačnění má pro udržení stálé glykemie velký význam rozklad jaterního glykogenu. Glykogenolýza a glukoneogeneze jsou aktivovány díky vzestupu hladin glukagonu (zejm. při hladovění), kortisolu a adrenalinu (při fyzické zátěži a stresu) a poklesu hladin insulinu. Dále jsou v důsledku inhibice lipogeneze laktát, pyruvát a aminokyseliny, které by byly touto drahou využity, přesměrovány do syntézy glukosy. Coriho cyklus a alaninový cyklus se tak stávají důležitými drahami pro udržení konstantní glykemie. Degradace aminokyselin jako zdroje energie je v časných fázích lačnění výrazně potlačena, protože chybí dodávka aminokyselin ze střeva. V důsledku aktivace glykogenolýzy a glukoneogeneze stoupá tvorba glukosa-6-fosfátu, který je glukosa-6-fosfatasou přeměněn na glukosu (reakce glykolýzy a syntézy glykogenu jsou zablokované). Zvýšení intracelulární koncentrace glukosy v hepatocytech umožní její transport usnadněnou difuzí z buňky do krve (Obr. 14).
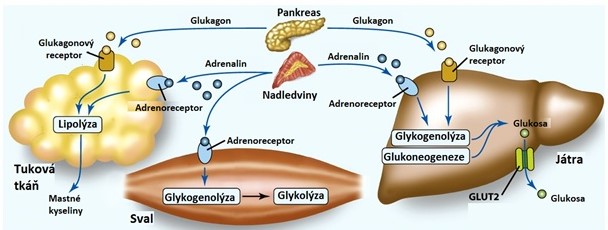
Obr. 14. Hormonální regulace metabolismu glukosy ve stavu lačnění/stresu (upraveno z Corkill 2017)
Při delším hladovění chybí dodávka živin ze střeva a v játrech zbývá jen málo glykogenu, proto jsou tkáně využívající glukosu závislé na jaterní glukonoegenezi, jejímiž zdroji jsou zejména laktát, glycerol a alanin. Avšak Coriho cyklus a alaninový cyklus neposkytují dostatek uhlíků pro celkovou syntézu glukosy. Glukosa vytvořená z laktátu a alaninu pouze nahradí tu, která je periferními tkáněmi přeměněna na laktát a alanin. Mozek však oxiduje glukosu až na CO2 a H2O. Proto je během hladovění potřeba ještě další zdroj uhlíků pro syntézu glukosy. Takovým zdrojem je jednak glycerol pocházející z degradace lipidů (acetyl-CoA nemůže být přeměněn na tříuhlíkatý intermediát glukoneogeneze!), a také aminokyseliny alanin, glutamin a glycin pocházející z rozkladu svalových proteinů. Ze svalů jsou uvolněny také 2‑oxokyseliny s rozvětveným řetězcem (degradační produkty větvených aminokyselin), které v játrech slouží jako substrát pro syntézu glukosy (valin a izoleucin) a ketolátek (leucin a izoleucin).
Hodnocení schopnosti organismu regulovat glykemii
U řady onemocnění není organismus schopen udržet konstantní glykemii. Konečným důsledkem zhoršené glukosové tolerance, ke které dochází např. při chronickém přejídání, stresu, obezitě, cirrhose jater či chronické nedostatečnosti ledvin, může být vznik diabetu mellitu. Protože stanovení lačné glykemie (FPG, fasting plasma glucose) není vždy spolehlivým ukazatelem schopnosti organismu regulovat hladinu glukosy, používají se další biochemické ukazatele – hladina glykovaného hemoglobinu a orální glukosový toleranční test. Při hodnotách glykemie v rozmezí 5,6-7 mmol/l hovoříme o poruše glukosové tolerance (IFG, impaired fasting glucose) či prediabetu.
Glykovaný hemoglobin v krvi (HbA1c) je dlouhodobým ukazatelem glykemie za posledních 8-12 týdnů a představuje vhodný způsob kontroly koncentrací glukosy u diabetiků, neboť je považován za její vážený dlouhodobý průměr. Používá se rovněž pro screening prediabetu. Referenční rozmezí je 20-42 mmol/mol, což představuje 4-6 % celkového hemoglobinu. Při dekompenzovaném diabetu jsou hodnoty HbA1c vyšší než 7 % z celkového obsahu hemoglobinu v krvi.
Orální glukosový toleranční test (oGTT) se používá k potvrzení diagnosy DM v případě, že diagnóza není jednoznačně potvrzena nálezem FPG vyšším než 7,0 mmol/l, a k diagnostice gestačního DM. Používá se zátěž 75 g glukózy a hodnotí se koncentrace glukosy v plasmě před zátěží a 2 hodiny po zátěži (u gestačního DM ještě 1 hodinu po zátěži). Nejprve dochází ke vzestupu glykemie, která dosahuje maxima během 60 minut po zátěži. Pak hladina glukosy zvolna klesá a k její normalizaci dochází do dvou hodin od jejího příjmu. Za fyziologických podmínek by glykemie neměla překročit ledvinový práh (cca 10 mmol/l) a neměla by se tedy objevit v moči. U pacientů s DM je FPG zvýšená a po zatížení glukosou překračuje glykemie transportní kapacitu ledvin a vzniká glykosurie. Glykemie dosahuje maximálních hodnot později a rovněž návratu na výchozí hodnoty je dosaženo později. U prediabetu je FPG normální, ale po zátěži glukosou se objevuje charakteristický průběh „diabetické“ křivky (Obr. 15).
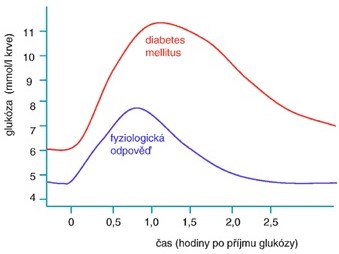
Obr. 15. Orální glukosový toleranční test (převzato z Holeček 2006)