Poruchy katabolismu a vylučování hemu - ikterus
Hyperbilirubinemie
Z přehledu katabolismu hemu a vylučování jeho produktů je zřejmé, že takovýto několikastupňový metabolický a vylučovací proces může být v jednotlivých krocích postižen defekty nebo kvantitativními změnami. Charakteristickým znakem patologických změn v katabolismu hemu a vylučování bilirubinu je zvýšená koncentrace bilirubinu v krvi – hyperbilirubinémie. Podle toho, který krok tohoto procesu je postižen, je hyperbilirubinémie způsobena buď vysokou koncentrací bilirubinu ještě nekonjugovaného (nerozpustného ve vodě), nebo bilirubinu konjugovaného (rozpustného ve vodě), případně obou forem. Rozlišení typu hyperbilirubinémie a její kvantifikace je významným diagnostickým prostředkem biochemické laboratoře. Sledování koncentrace bilirubinu v krevním séru nebo plasmě je významným diagnostickým prostředkem, zejména při poškození jater („jaterní testy“).
K rozlišení obou typů bilirubinu slouží reakce s diazotovanou kyselinou sulfanilovou. Reakce byla původně zavedena Ehrlichem v roce 1883. Existuje několik modifikací a běžně se používá název van den Berghova reakce podle holandského lékaře, který ji začal uplatňovat v diagnostice žloutenek. Van den Berghova reakce se v biochemické laboratoři nejčastěji provádí v modifikaci podle Jendrassika a Grófa s fotometrií při vlnové délce 520-550 nm.
Kromě van den Berghovy reakce se používá k stanovení bilirubinu několik dalších metod, jako je přímá fotometrie nebo enzymatické stanovení bilirubinu přeměnou na biliverdin za katalýzy bilirubinoxidasou (změna absorpce při 405-460 nm).
Konjugovaný bilirubin reaguje s diazočinidlem okamžitě (tzv. přímý bilirubin). Spolu s konjugovaným bilirubinem reaguje jako přímý bilirubin také asi 10-15 % nekonjugovaného bilirubinu (Obr. 24).
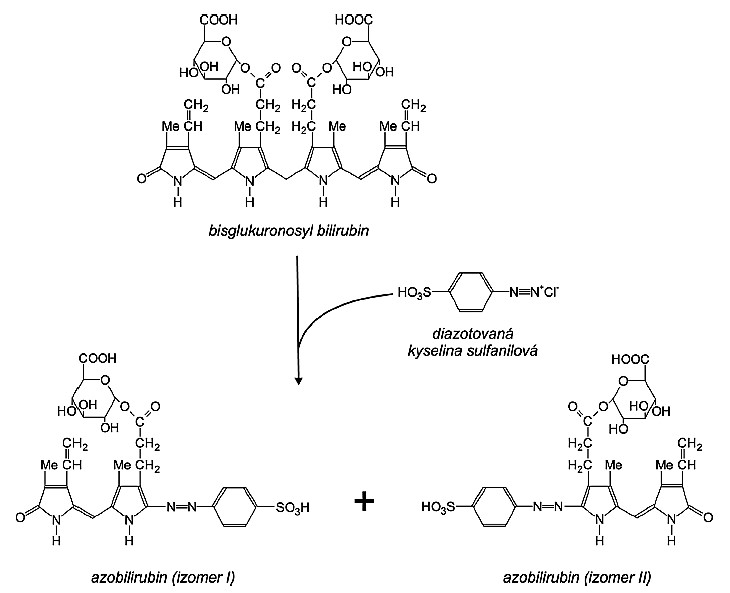
Obr. 24. Reakce konjugovaného bilirubinu s diazotovanou kyselinou sulfanilovou (Vítek 2009)
Jinak musí být nekonjugovaný bilirubin nejprve rozpuštěn např. přidáním methanolu nebo jiného „akcelerátoru“ (kofein, kyselina benzoová…). Po přidání akcelerátoru se získá celková koncentrace bilirubinu ve vyšetřovaném séru (celkový bilirubin).
Odečtením hodnoty přímého bilirubinu od celkového bilirubinu se získá hodnota nepřímého bilirubinu. Nepřímý bilirubin je hodnota vypočtená, nikoliv naměřená. Představuje asi 85-90 % nekonjugovaného bilirubinu.

Obr. 25. Přímý a nepřímý bilirubin na základě van den Berghovy reakce (upraveno z Memorangapp.com 2019)
Ikterus (žloutenka)
Normální koncentrace bilirubinu v séru nebo plasmě je 2,0–17,0 µmol/l. Hyperbilirubinemie je zvýšení hladiny bilirubinu v krvi nad 25 μmol/l. Jestliže koncentrace bilirubinu v krvi překročí určitou hodnotu, přebytečný bilirubin difunduje do tkání, které tím zežloutnou. Ikterus (žloutenka) je žluté zbarvení sklér, později i kůže a sliznic, které je patrné obvykle při hodnotách nad 68–85 µmol/l. K tomu může dojít ze různých příčin, které je třeba identifikovat.
Podle lokalizace příčiny ikteru z hlediska vztahu k játrům se žloutenky dělí klasicky do tří skupin (Obr. 26):
- prehepatální (hemolytický) ikterus
- hepatální (hepatocelulární)
- posthepatální (obstrukční)
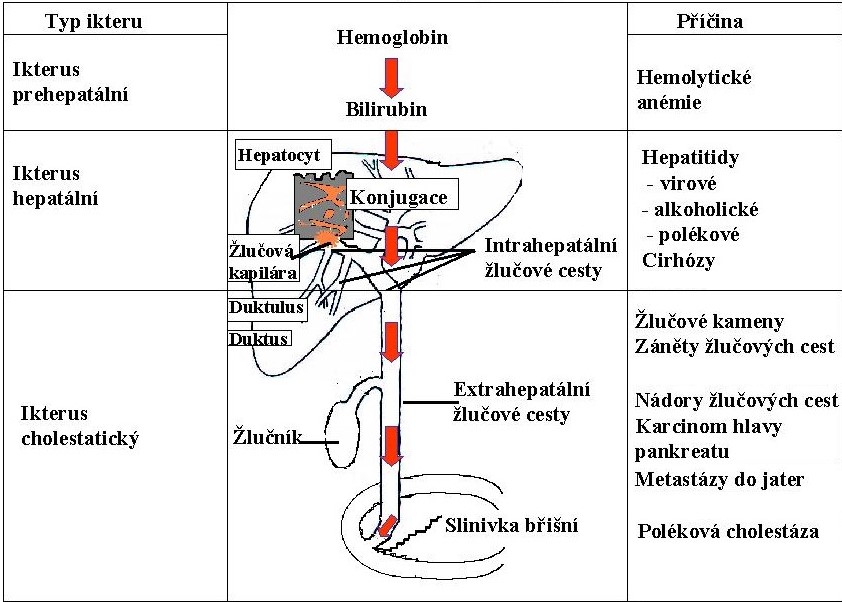
Obr. 26. Typy ikteru a jejich příčiny (upraveno z Ehrmann a Krtek 2002)
Prehepatální ikterus
Typickou příčinou prehepatálního ikteru je hemolytická anémie, kdy dochází ke zvýšenému rozpadu erytrocytů. Zvýšená nabídka hemoglobinu z rozpadajících se erytrocytů vede k hyperbilirubinemii, způsobené nekonjugovaným bilirubinem, který se nevylučuje do moči. Zdravá játra jsou schopna nabídnutý bilirubin konjugovat a vyloučit. Zvýšený obsah bilirubinu ve střevě vede ke zvýšené tvorbě sterkobilinu. Žloutenka má zlatožlutý, slámově‑žlutý odstín. Barva moči je normální, žluč je tmavá, stolice je tmavá, hypercholická. V důsledku větší nabídky urobilinogenu (reabsorpce za střeva) bývá v moči přítomen urobilinogen (Obr. 27).
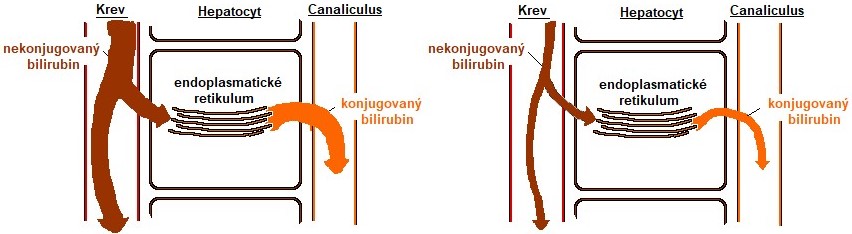
Obr. 27. Prehepatální (hemolytický) ikterus (vlevo) ve srovnání s normálním stavem (vpravo) (upraveno z Baggott a Dennis 1994)
Hepatální ikterus
Jeho obraz může být pestřejší podle toho, jaká porucha hepatocytu je jeho příčinou.
- Ikterus premikrosomální
- Bilirubin nabízený z krve játrům buď není dostatečně transportován do hepatocytu, nebo není dostatečně přenášen do endoplasmatického retikula (mikrosomální buněčná frakce). V tomto případě se nekonjugovaný bilirubin hromadí v krvi a způsobuje zvýšení nepřímé hyperbilirubinémie podobně, jako u prehepatálního (hemolytického) ikteru.
- Ikterus mikrosomální
- Bilirubin není dostatečně konjugován. Defekt působí nepřímou hyperbilirubinémii podobně jako předchozí typy (Obr. 28)
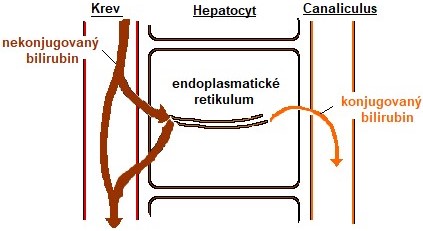
Obr. 28. Hepatální mikrosomální ikterus (upraveno z Baggott a Dennis 1994)
- Ikterus postmikrosomální
- Bilirubin je konjugován, avšak vázne jeho další přesun do žluči (vnitřní – intrahepatální obstrukce). Konjugovaný bilirubin přestupuje do krve a způsobuje přímou hyperbilirubinémii. Konjugovaný bilirubin je relativně malá molekula, která se v glomerulech nezachytí a objevuje se v moči. Žloutenka má rubínový odstín, moč je tmavá, žluč je světlá, stolice světlejší než normálně (Obr. 29).
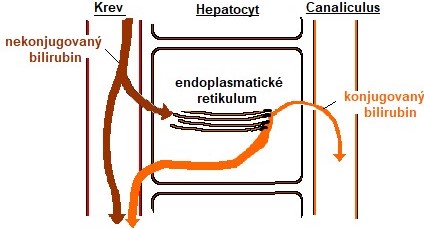
Obr. 29. Hepatální postmikrosomální ikterus (intrahepatální obstrukce) (upraveno z Baggott a Dennis 1994)
Hepatální ikterus vzniklý poškozením hepatocytů (hepatocelulární ikterus) může být kombinací všech tří výše uvedených typů. Hyperbilirubinémie je způsobena zvýšením jak nekonjugovaného, tak konjugovaného bilirubinu.
Častými příčinami jaterního poškození s hyperbilirubinémií a žloutenkou jsou např. hepatitidy nebo jaterní cirhóza. Většinou převládá biochemický obraz obstrukce a může se řadit k obstrukčním žloutenkám.
Posthepatální (obstrukční) ikterus
Obstrukční žloutenka je způsobena zpravidla žlučovými kameny (cholelithiáza), blokujícími úplně nebo částečně vývodné žlučové cesty, méně často je obstrukce způsobena nádorem (Obr. 30).
Odstín ikteru je zelenožlutý až černý. Moč je tmavá, stolice světlá, při úplné obstrukci odbarvená – acholická. V séru je zvýšen bilirubin konjugovaný. V moči při úplné obstrukci se prokáže bilirubin, ale není přítomen urobilinogen. Nápadným příznakem cholestázy je svědění kůže.
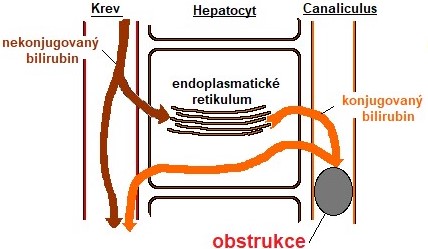
Obr. 30. Posthepatální (obstrukční) ikterus (upraveno z Baggott a Dennis 1994)
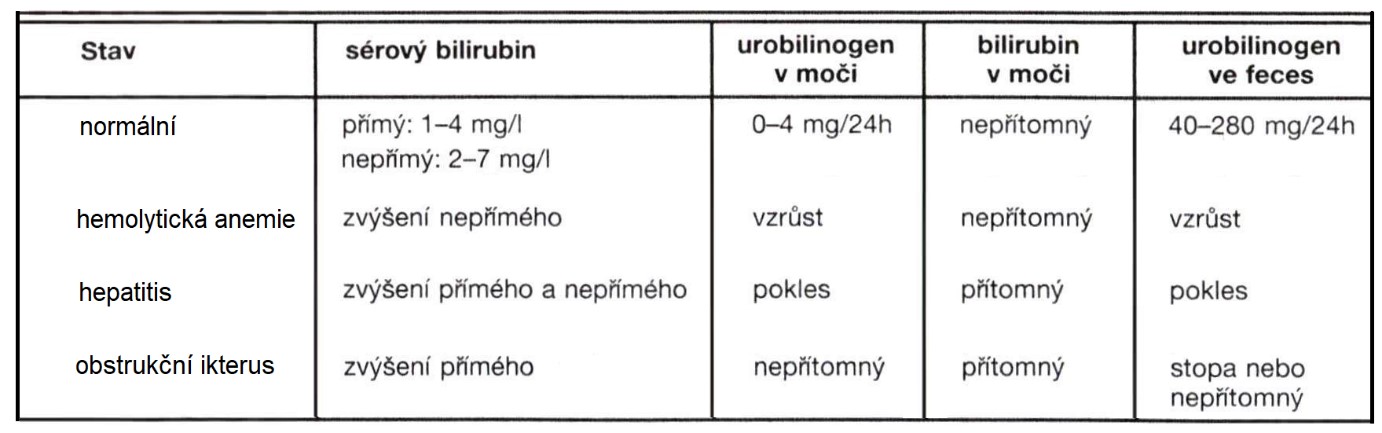
Příklady laboratorních nálezů u vybraných typů ikterů jsou uvedeny v Tab. 4.
Tab. 4. Příklady laboratorních nálezů u různých typů ikteru (upraveno z Muray et al. 1998)
Novorozenecká žloutenka
Asi u poloviny novorozenců se objeví žloutenka během prvních pěti dnů života. Příčinou je zejména nízká aktivita jaterní UDP-glukuronosyltransferasy, tedy enzymu katalyzujícího konjugaci bilirubinu. U novorozenců představuje aktivita tohoto enzymu asi jen 1 % aktivity u dospělých, během dalších dnů rychle stoupá a dosáhne plné aktivity do 14 dnů. Dalšími přispívajícími faktory jsou např.:
- vyšší rozpad erytrocytů po narození, čímž vzniká najednou velké množství bilirubinu,
- nižší aktivita glutathion-S-transferasy, což se projeví jako nižší příjem a záchyt bilirubinu v hepatocytech
- nižší tvorba albuminu, potřebného pro transport nekonjugovaného bilirubinu v krvi (nezralost jater u novorozence).
Novorozenecký ikterus se objevuje i u zralých donošených novorozenců jako fyziologická novorozenecká žloutenka. U nedonošenců, kde je nezralost jednotlivých složek systému výraznější, je žloutenka výraznější a může ohrozit novorozence (Obr. 31).
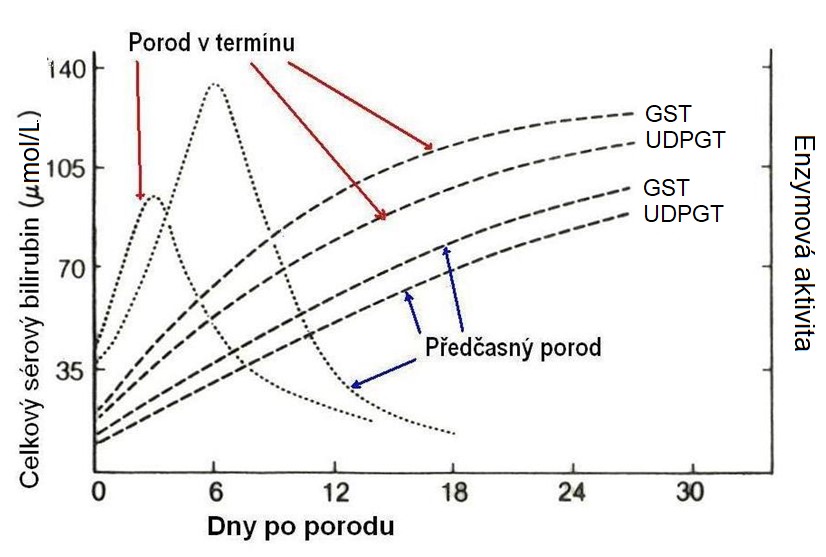
Obr. 31. Průběh koncentrace bilirubinu a enzymové aktivity v séru novorozence (upraveno z Gornall 1986). GST = glutathion-S-transferasa; UDPGT = UDP-glukuronosyltransferasa.
Volný bilirubin, tj. ta část nekonjugovaného bilirubinu, která není navázána na albumin, je toxický pro CNS. Ukládáním volného bilirubinu do mozkové tkáně, bazálních ganglií a mozkového kmene může vzniknout tzv. Kernikterus (jádrový ikterus, z němčiny), který je velmi závažnou, naštěstí vzácnou komplikací hyperbilirubinemie.
Toxicitu bilirubinu ovlivňuje řada faktorů – gestační věk, etnicita, přítomnost hemolýzy, asfyxie, acidóza, hypoperfuze, hyperosmolalita, sepse. Nejprve se objevují mírné, nespecifické příznaky toxického působení bilirubinu na centrální nervový systém, jako je letargie, hypotonie problémy s krmením a pláč. Rozvinutý jádrový ikterus se projevuje jako encefalopatie ve formě mozkové obrny (atetoidní forma), postupně mentální retardace, poruchy sluchu až hluchota, paralýza okohybných svalů.
Terapie novorozenecké žloutenky cílí k snížení koncentrace bilirubinu. Podílí se i farmakoterapie a výměnné transfuze krve, avšak základním a snadným terapeutickým postupem je fototerapie. Fototerapeuticky nejúčinnější je modré světlo (nikoliv UV), jehož vlnová délka je nejblíže absorpčnímu spektru bilirubinu (460 nm), jehož působením se ruší vodíkové můstky, molekula bilirubinu se otvírá, stává se rozpustnou ve vodě a vylučuje se močí, aniž by musel být konjugován Obr. 32).
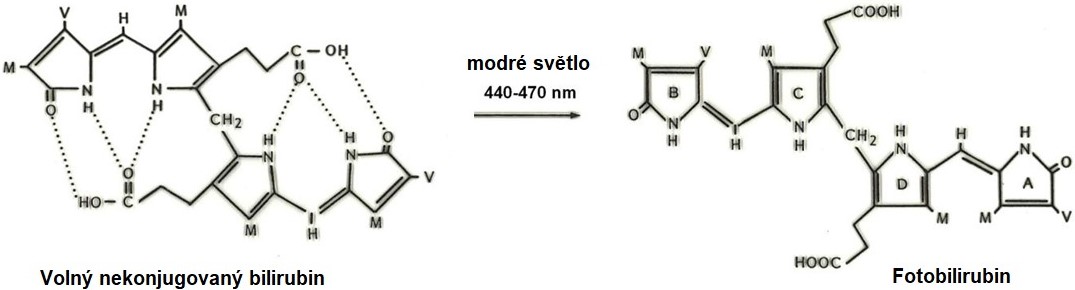
Obr. 32. Vznik fotobilirubinu působením modrého světla (upraveno z Gornall 1986).
Dědičné hyperbilirubinémie
Jedná se o skupinu metabolických onemocnění, charakterizovaných zvýšenou hladinou celkového bilirubinu nebo jeho konjugované frakce v séru. Většina z těchto poruch je děděna autosomálně recesivně a manifestuje se zejména v mladém věku. Příčinou jsou poruchy konjugace bilirubinu nebo jeho transportu. Schematické porovnání tří nejčastějších typů dědičných hyperbilirubinemií je uvedeno v Obr. 33.
Gilbertův syndrom
Toto onemocnění je dědičnou poruchou metabolismu žlučového barviva bilirubinu v krvi. Je způsobeno geneticky podmíněným defektem glukuronidace bilirubinu. Příčinou je porucha TATAA boxu promotorové oblasti genu pro UDP-glukuronosyltransferasu, jejímž výsledkem je snížení exprese a následně aktivity jaterního enzymu asi na 30 % normální aktivity. Onemocnění je autosomálně recesivní a vyskytuje se u 3-15 % indoevropské populace (u nás asi 5 %). Projevuje se zežloutnutím kůže a očního bělma v důsledku ukládání přebytečného bilirubinu do tkání. Hyperbilirubinémie je způsobena chronickým mírným zvýšením nekonjugovaného bilirubinu (17-100 μmol/l). Toto onemocnění nezkracuje délku ani nesnižuje kvalitu života, naopak se mírná hyperbilirubinemie vzhledem k antioxidačním účinkům bilirubinu považuje za výhodu.
Criglerův-Najjarův syndrom I. typu
Jedná se o velmi vzácné autosomálně recesivní onemocnění s úplným defektem UDP‑glukuronosyltransferasy (asi 200 případů v celém světě) na základě několika různých mutací. Způsobuje těžkou nekonjugovanou hyperbilirubinémii. Vzestup bilirubinu je prudký už během prvních hodin života. Závažnou komplikací je jádrový ikterus. Syndrom se léčí transfuzemi krve, fototerapií (účinek postupně klesá), inhibitory hemoxygenasy (zpomalení tvorby bilirubinu), podáváním látek komplexujících bilirubin, transplantací jater. Bez léčby umírají postižení do 18 měsíců života.
Existuje mírnější forma – Criglerův-Najjarův syndrom II. typu, kdy aktivita jaterní UDP-glukuronosyltransferasy je snížena částečně. Léčí se fenobarbitalem, který indukuje cytochrom P450.
Dubin-Johnsonův syndrom
Tento syndrom je opět vzácný, autosomálně recesivní. Je způsoben defektem transportéru MRP2 (kasetový „multidrug resistence-associated protein 2“), jehož úkolem je transportovat konjugovaný bilirubin do žlučového vývodu. Je zachováno asi na 10 % normální transportní aktivity. Jaterní funkce není poškozena. Na rozdíl od předchozích dvou dědičných hyperbilirubinémií je Dubin-Johnsonův syndrom charakterizován zvýšením konjugovaného bilirubinu.
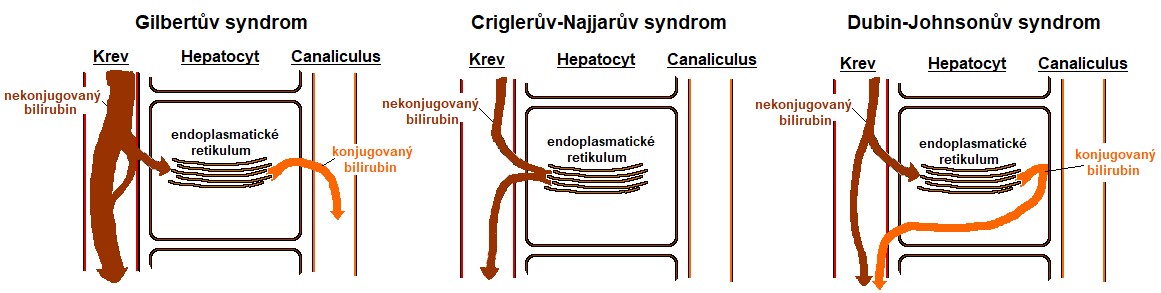
Obr. 33. Schematické srovnání dědičných hyperbilirubinemií (upraveno z Baggott a Dennis 1994).