Vstřebávání lipidů
Vstřebávání lipidů se odehrává hlavně v horní části tenkého střeva, kde se absorbuje více než 95 % přijatých tuků. Pohybem tráveniny se dostávají micely do kontaktu se střevní sliznicí. Na povrchu mikroklků dochází k přilnutí micel k plazmatické membráně enterocytů. Monoacylglyceroly, cholesterol a mastné kyseliny se začnou v membráně enterocytu rozpouštět a procesem difúze pronikají dovnitř buňky. Děj probíhá jednak mechanismem prosté difúze, především však mechanismem usnadněné difúze pomocí přenašeče FATP („fatty acids transporting protein“, transportní protein pro mastné kyseliny). Existuje nejméně 6 různých FATP lokalizovaných v buňkách kosterního svalstva, tukové tkáně a střeva, z nichž některé vykazují acyl-CoA-syntetasovou aktivitu. Díky tomu jsou schopny aktivovat mastné kyseliny a podle momentální potřeby buňky umožnit jejich esterifikaci nebo oxidaci. Část vstřebaného cholesterolu se prakticky ihned vrací z enterocytu zpět do lumen střeva. K tomu buňka využívá přenašeč označený jako ABCA1, známý též jako CERP („cholesterol efflux regulatory protein“).
Zbytek rozpadlých micel je tráveninou posouván až do ilea, kde jsou aktivně vstřebávány žlučové kyseliny. Ty jsou pak portální krví přivedeny do jater a enterohepatální cirkulací opět do žluče. Nerozložené triacylglyceroly nebo diacylglyceroly jsou ve střevě vstřebávány velice špatně. Není to z důvodů jejich velikosti molekuly nebo tím, že by špatně do enterocytu difundovaly, ale nejsou součástí micel a neúčastní se tedy procesu splynutí micely s buněčnou membránou enterocytu. Tím se ukazuje mimořádná důležitost enzymu pankreatické lipasy a s ní spojené správné fungování kolipasy. Bez jejich správné funkce nevzniknou potřebné 2‑monoacylglyceroly, které jsou základem pro vznik micel.
Vstřebané monoacylglyceroly (příp. i diacylglyceroly) jsou intracelulárními lipasami štěpeny na glycerol a volné mastné kyseliny. Průchod MK enterocytem je závislý na délce řetězce mastné kyseliny. Pokud molekula MK obsahuje v řetězci více než 10 atomů uhlíku (MK s dlouhým řetězcem - LCT, „Long Chain Triglycerides“), je využita k opětovné syntéze nových triacylglycerolů. Tyto TAG se pak na bazální straně enterocytů vylučují ve formě chylomiker do lymfy. Mastné kyseliny s nižším počtem atomů uhlíku (MK se středně dlouhým řetězcem - MCT, „Middle Chain Triglycerides“) prochází enterocytem k bazální straně beze změny, jsou přenášeny přímo do portální krve a jsou vychytávány jaterními buňkami.
Resyntéza triacylglycerolů v enterocytu
Většina vstřebaných mastných kyselin je uvnitř enterocytu využita pro opětovnou syntézu triacylglycerolů nebo pro esterifikaci cholesterolu (Obr. 8). V cytosolu enterocytů se nachází speciální protein (FABP, „fatty acids binding protein“), který na sebe váže vstřebané mastné kyseliny a transportuje je směrem k hladkému endoplazmatickému retikulu. Na rozdíl od jiných tkání probíhá syntéza triacylglycerolů v enterocytu monoacylglycerolovou dráhou, tedy na základě 2-monoacylglycerolů. Jak bylo popsáno výše, právě tyto struktury vznikají rozkladem triacylglycerolů ve střevě a jsou tedy do enterocytu dodávané v odpovídajícím množství. V hladkém endoplazmatickém retikulu pak dochází k syntéze 1,2-diacylglycerolů (reakci katalyzují monoacylglyceroltransferasy) a následně k syntéze triacylglycerolů (reakci katalyzují diacylglyceroltransferasy). Tím, že se mastné kyseliny znovu používají k syntéze triacylglycerolů a jsou neustále vychytávány FABP, vzniká potřebný gradient pro vstřebávání dalších molekul monoacylglycerolů a volných mastných kyselin z lumen střeva do cytosolu enterocytů. Mastné kyseliny vázané na FABP mohou působit jako signální molekuly a ovlivňovat receptory v buněčném jádře (stimulace syntézy apoproteinů B).
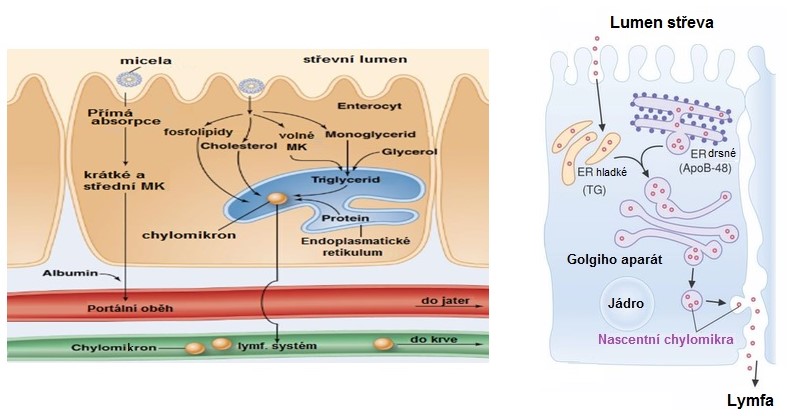
Obr. 8. Resyntéza triacylglycerolů a tvorba chylomiker v enterocytu (upraveno z Thompson et al. 2011 a Lieberman a Marks 2013)
Produkty trávení lipidů jsou v enterocytech „zabaleny“ do částic, nazývaných chylomikra (Obr. 8). Základem pro tvorbu chylomiker je syntéza speciálních proteinů v ribosomech enterocytů, zejména apolipoproteinu B-48 (a rovněž apoproteinů A-I, A-II, A-IV). Apoproteiny jsou přenášeny do tubulů hladkého endoplazmatického retikula, kde se spojují s vytvářenými triacylglyceroly. Vzniká tak základ budoucích lipoproteinových komplexů označovaných jako chylomikra. Vytvářející se jádro chylomikronové částice je transportováno do Golgiho aparátu, kde dochází k navázání sacharidových zbytků. Na své cestě Golgiho aparátem směrem k buněčné membráně přibírají cholesterol a také polární fosfolipidy, které spolu s apoproteiny dotváří povrch vznikajících chylomiker. Ve formě sekrečních váčků jsou zformovaná chylomikra posouvána cytoplazmou směrem k buněčné membráně. Buňku pak opouští fúzí sekreční vakuoly s buněčnou membránou (proces reverzní pinocytózy). Chylomikra postupují do lymfatického systému a do krve jsou vypuštěna přes ductus thoracicus do hrudní žíly. Důvod pro tuto cestu je především v tom, že chylomikra jsou příliš velká na to, aby byla schopna přestoupit přímo do krve přes endotel kapilár. Tato cesta má zároveň význam pro osud triacylglycerolů transportovaných v chylomikrech. Tím, že obejdou játra, dostávají se přednostně do svalů. Pokud by se vstřebaly přímo do portální krve, procházely by nejprve játry, kde by se začleňovaly do lipoproteinové frakce určené především pro přesun do tukové tkáně.
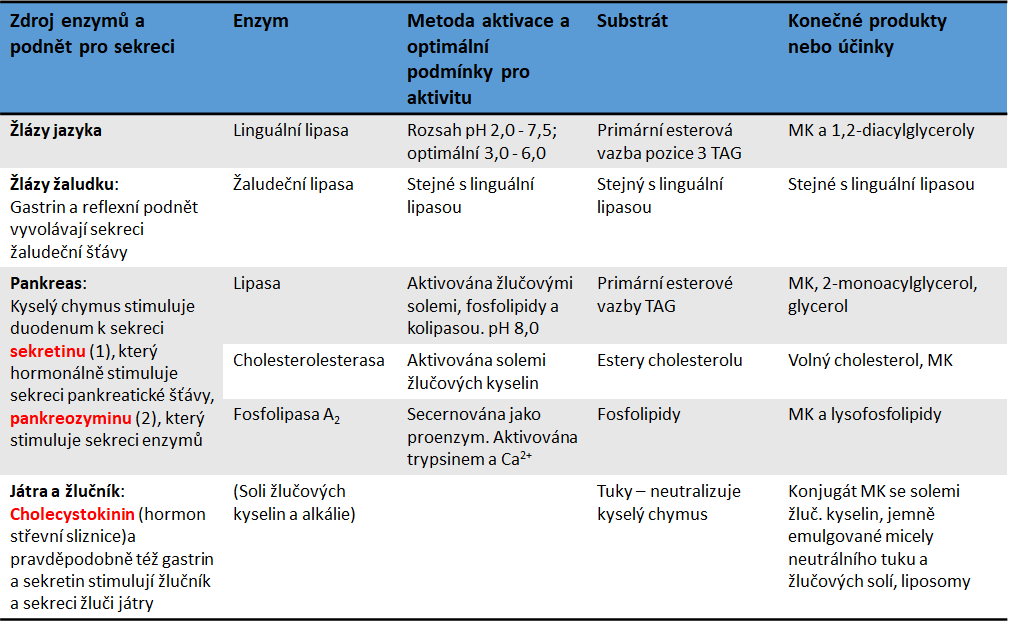
Přehled trávicích procesů probíhajících v GIT, přehled lipas a jejich funkce v trávicím traktu jsou sumarizovány v Tab. 3.
Tabulka 3. Přehled lipas a jejich funkce v trávicím systému