Mediátory zánětu
Mediátory zánětu zprostředkují odpověď organismu na cizorodý stimul. Jedná se rozpustné sloučeniny schopné difúze, které aktivují některou ze složek zánětu prostřednictvím interakce s příslušným receptorem. Působí lokálně i na vzdálenějších místech organismu. Endogenní mediátory vznikají působením imunitního a hemokoagulačního systému, zatímco exogenní mediátory jsou sloučeniny vytvořené původci infekce, fyzikálními faktory či mechanickými vlivy. Působí jako faktory vasopermeability (kininy, eikosanoidy, histamin, serotonin, anafylatoxiny komplementu) nebo leukotaktické faktory (peptidy komplementu, bakteriální produkty, štěpné produkty fibrinu, cytokiny). Endogenní mediátory zánětu můžeme podle původu rozdělit na plazmatické, které jsou syntetizované v játrech, a buněčné pocházející z neutrofilů, monocytů/makrofágů, žírných buněk, destiček či endotelových buněk (Obr. 1).
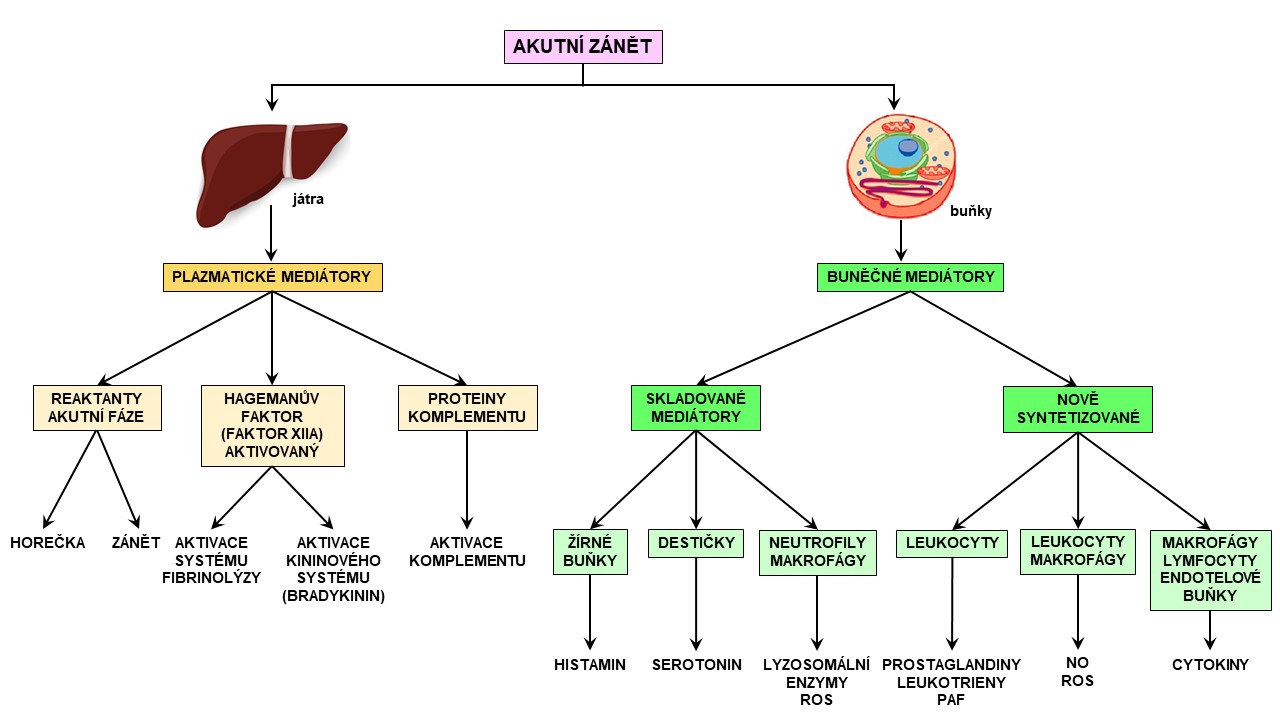
Obr. 1: Plazmatické a buněčné mediátory zánětu (upraveno z Porth 2011).
Mediátory časné fáze mají význam hlavně v akutní zánětlivé reakci a patří mezi ně histamin, serotonin a další vazoaktivní látky syntetizované žírnými buňkami a destičkami, chemoatraktanty (např. C5a) a cytokiny (interleukin-1, interleukin-6, tumor-nekrotizující faktorα). Mediátory pozdní fáze regulují vaskulární změny, které se odehrávají později (cca 6-12 hodin po iniciaci zánětu). Patří mezi ně zejména lipidové mediátory tvořené z kyseliny arachidonové.
Histamin a serotonin
Nejvýznamnějšími vazoaktivními mediátory zánětu jsou biogenní aminy histamin a serotonin (větší význam u hlodavců). Jsou skladovány v granulech žírných buněk, bazofilů a destiček. Histamin vzniká dekarboxylací aminokyseliny histidinu, která je katalyzovaná histidindekarboxylasou. V granulech žírných buněk vytváří komplexy s glykosaminoglykanem heparinem (součást proteoglykanu serglycinu). Po degranulaci žírných buněk je exocytózou uvolněn do okolí, kde vyvolává dilataci arteriol, zvýšení vaskulární permeability, kontrakci hladkých svalů (např. bronchů) a působí jako chemoatraktant pro eozinofily. Tyto účinky jsou zprostředkovány interakcí histaminu s H1 receptory. Histamin je degradován oxidační deaminací, kterou katalyzuje enzym histaminasa (diaminoxidasa) na imidazolacetát. Serotonin vzniká z aminokyseliny tryptofanu, který je nejprve tryptofanhydroxylasou hydroxylován v poloze 5 na 5-hydroxytryptofan. Ten je následně dekarboxylován na serotonin pomocí dekarboxylasy aromatických aminokyselin. Rovněž serotonin zvyšuje vaskulární permeabilitu, vyvolává dilataci kapilár a kontrakci hladkých svalů (mimo cévy). Jeho vazokonstrikční účinek snižuje únik krve z těla při krvácivých poraněních. Většina serotoninu je uložena v GITu a CNS, ale velké množství je uloženo rovněž v granulech destiček. Hlavní degradační drahou serotoninu je oxidační deaminace monoaminoxidasou A na 5‑hydroxyindolacetaldehyd a následná oxidace aldehyddehydrogenasou na 5‑hydroxyindolacetát.
Kallikrein-kininový systém
Kininy (bradykinin, kallidin) jsou významnými mediátory zánětu peptidové povahy. Vznikají z molekul prekurzorů (kininogenů) působením proteolytických enzymů (např. kallikreinu). Kininogeny jsou syntetizovány játry a uvolněny do krve, kde působí jako kofaktory hemokoagulační kaskády, inhibitory cysteinových proteas a jako součást reakce akutní fáze. Kallikrein je v plazmě přítomen v neaktivní formě, která se označuje jako prekallikrein, a tvoří komplex s vysokomolekulárním kininogenem (HMW kininogen). Při poškození tkáně, kdy dochází k odkrytí kolagenních vláken, se tento komplex spolu s Hagemanovým faktorem (faktor XII krevního srážení) váže na negativně nabitý kolagen. Hagemanův faktor je aktivován a štěpí prekallikrein na kallikrein, čímž ho aktivuje. Kallikrein rozkládá vysokomolekulární kininogen za vzniku nonapeptidu bradykininu. Bradykinin je silným vasoaktivním mediátorem, který zvyšuje vaskulární permeabilitu, vyvolává vasodilataci, bolest a stimuluje metabolismus kyseliny arachidonové. Aktivita a vznik bradykininu jsou pečlivě kontrolovány. Aktivace kininové dráhy může být potlačena působením inhibitorů aktivovaného Hagemanova faktoru (C1 inhibitor) nebo kallikreinu (C1 inhibitor, α2-makroglobulin). Navíc je v plazmě přítomná řada enzymů, které bradykinin rozkládají a snižují tak jeho aktivitu. Mezi ně patří například angiotenzin-konvertující enzym a karboxypeptidasa N, které se označují jako kininasy (Obr. 2).
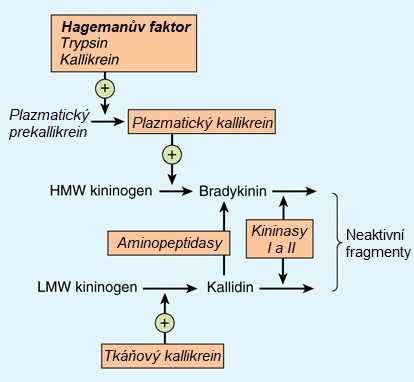
Obr. 2. Kallikrein-kininový systém (upraveno z Katzung a kol. 2012). HMW kininogen = vysokomolekulární kininogen, LMW kininogen = nízkomolekulární kininogen
Lipidové mediátory
Lipidové mediátory můžeme rozdělit do dvou skupin – na eikosanoidy a plasmalogeny (Obr. 3). Během zánětu jsou aktivovány buněčné fosfolipasy (zejm. fosfolipasa A2), které membránové fosfolipidy štěpí a uvolňují arachidonát. Zbývající lysofosfolipid (lyso-PAF) je acetyltransferasou přeměněn na faktor aktivující destičky (PAF), který patří do skupiny plasmalogenů. Arachidonát má krátký biologický poločas a může být metabolizována dvěma hlavními cestami – cyklooxygenasovou a lipoxygenasovou – za vzniku různých eikosanoidů. Působením cyklooxygenasy vznikají tzv. prostanoidy, mezi něž patří prostaglandiny, tromboxany a prostacyklin. Druhou cestou vznikají leukotrieny (katalyzováno 5-lipoxygenasou), hepoxiliny a 12-HETE (katalyzováno 12-lipoxygenasou), lipoxiny a 15-HETE (katalyzováno 15-lipoxygenasou). Lipidové mediátory nejsou v buňce skladovány, ale jsou syntetizovány a uvolněny v odpověď na odpovídající stimul. Jejich účinky v organismu se liší nejen podle druhu eikosanoidu, ale i podle toho, na které receptory může v daném místě působit.
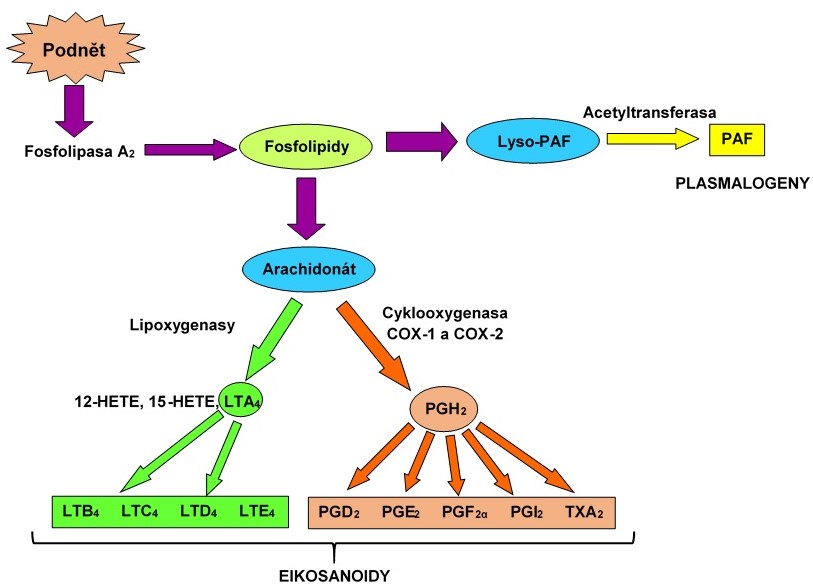
Obr. 3. Syntéza lipidových mediátorů.
Syntéza prostanoidů je zahájena cyklooxygenasou (prostaglandin-endoperoxid-synthasa; COX), která přeměňuje arachidonát na prostaglandin H2 (PGH2), který je společným meziproduktem syntézy všech typů prostanoidů. COX katalyzuje první dvě reakce syntézy prostanoidů – cyklooxygenasovou reakci, při které vzniká bicyklický endoperoxid s hydroperoxylovou skupinou PGG2, a peroxidasovou reakci, při které je hydroperoxylová skupina PGG2 redukována na hydroxylovou skupinu PGH2. Jsou známy dvě isoformy enzymu COX-1 (exprimována konstitutivně) a COX-2 (exprese indukována cytokiny nebo růstovými faktory). Nestabilní PGH2 je působením dalších enzymů přeměňován na tromboxany, prostaglandiny a prostacyklin. O tom, který prostanoid vznikne, rozhoduje enzymová výbava dané buňky. Daný typ buňky většinou produkuje 1 konkrétní druh prostanoidu: destičky produkují téměř výhradně tromboxany, cévní endoteliální buňky především prostacyklin a buňky myokardu hlavně PGE2 a PGF2α. Prostaglandiny vznikají působením např. prostaglandin-D2-synthasy nebo prostaglandin-E2-synthasy. Jedná se o tkáňové hormony, které jsou aktivní již v nanomolárních koncentracích. PGE2 vyvolává vasodilataci, zvyšuje vaskulární permeabilitu, je pyrogenem a zvyšuje citlivost na bolestivé podněty. Syntéza tromboxanů (Tx) je v destičkách, monocytech a makrofázích katalyzována tromboxansynthasou. TxA2 vyvolává agregaci destiček, vasokonstrikci a bronchokonstrikci. Jeho účinky jsou antagonizovány působením prostacyklinu (PGI2), který je silným vasodilatátorem a brání agregaci destiček. PGI2 je syntetizován v endotelových buňkách působením prostacyklinsynthasy. Základní struktury prostanoidů jsou uvedeny v Obr. 4.
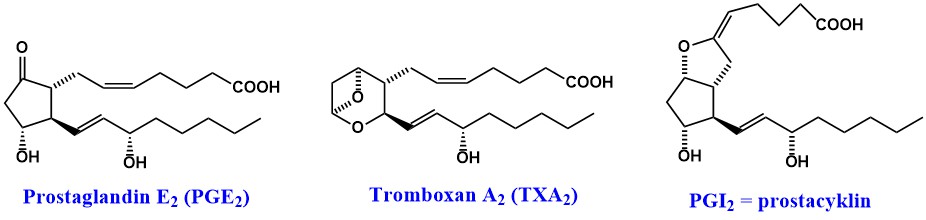
Obr. 4. Struktury základních prostanoidů.
Tři různé lipoxygenasy zavádějí kyslík do polohy 5, 12 či 15 arachidonátu, ale jen 5-lipoxygenasa syntetizuje leukotrieny (LT). Jedná se o dioxygenasy obsahující nehemové železo. Prvními vznikajícími produkty jsou hydroperoxyeikosatetraenové kyseliny (HPETE), které jsou rychle redukovány glutathionperoxidasou na hydroxyeikosatetraenové kyseliny (HETE) nebo podstoupí isomerizační reakce za vzniku leukotrienů či lipoxinů. 5-lipoxygenasa, je přítomná zejména v leukocytech a vyžaduje přítomnost aktivačního proteinu FLAP a Ca2+. Tento enzym katalyzuje přeměnu 5-HPETE na nestabilní LTA4, který je rychle přeměněn na peptidoleukotrieny (LTC4, LTD4 a LTE4) připojením molekuly GSH nebo hydrolyzován na LTB4. Leukotrieny jsou prozánětlivé mediátory, které působí v nízkých koncentracích (nM), vyvolávají rychlou odpověď organismu, ale jejich působení je krátkodobé. Mají vasokonstrikční a silný bronchokonstrikční účinek (zejm. peptidoLT), zvyšují permeabilitu cév, působí chemotakticky a aktivačně na leukocyty, podporují diapedézu a fagocytózu. Lipoxiny, na jejichž syntéze se podílí 15-lipoxygenasa, mají protizánětlivé účinky, podílejí se na odeznění zánětu a brání jeho přechodu do chronické fáze. Lipoxiny inhibují chemotaxi a diapedézu, brání produkci ROS a cytokinů, působí jako antagonisté receptorů pro LT, vyvolávají bronchodilataci. Hepoxiliny, které vznikají působením 12-lipoxygenasy, brání oxidačnímu poškození buněk zvýšením exprese GPx a stimulují sekreci insulinu v β-buňkách pankreatu. 5‑HETE se účastní imunitní obrany proti bakteriálním infekcím (participují na chemotaxi a degranulaci neutrofilů), zatímco 12-HETE a 15-HETE jsou syntetizované v ledvinách a podílejí se na regulaci angiotensin-aldosteronového systému. Základní strukturní vzorce jsou uvedeny v Obr. 5.
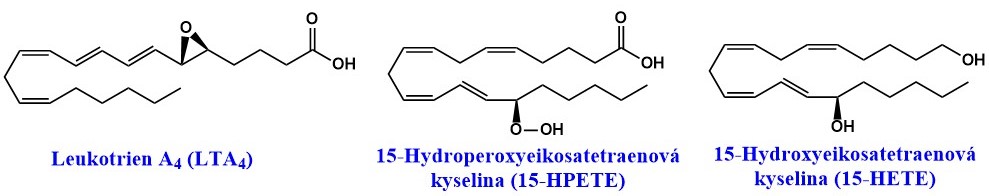
Obr. 5. Strukturní vzorce leukotrienu, HETE a HPETE.
Destičky produkují skupinu acetylovaných 1-O-alkyl-sn-glycerol-3-fosfocholinů označovaných jako faktor aktivující destičky (PAF). PAF vzniká acetylací lyso-PAF v poloze sn-2, kterou katalyzuje lyso-PAF-acetyltransferasa. Tento mediátor vyvolává agregaci destiček a to již v pikomolárních koncentracích, je silným chemoatraktantem pro fagocyty, stimuluje uvolnění lyzosomálních enzymů a tvorbu ROS v neutrofilech a makrofázích. Navíc zvyšuje adhezivitu endotelu pro leukocyty. Aktivita a koncentrace PAF jsou regulovány prostřednictvím PAF-acetylhydrolas, které odštěpují acetylovou skupinu PAF. Plazmatická isoforma PAF-acetylhydrolasy je nekovalentně připojena k lipoproteinovým částicím HDL a LDL, další dvě isoformy působí intracelulárně v buňkách ledvin, jater, mozku a červených krvinek.
Komplement
Komplement je komplexní systém složený z více než 30 glykoproteinů přítomných v krvi ve formě složek, faktorů a dalších regulátorů a/nebo na povrchu různých buněk ve formě receptorů. Složky komplementu jsou v krvi přítomné v neaktivní formě, které se kaskádovitě aktivují proteolytickým štěpením. Rozeznáváme tři dráhy aktivace komplementu – klasickou, alternativní a lektinovou, které se od sebe liší způsobem aktivace klíčové složky C3. Klasická dráha je aktivována imunokomplexy antigen-protilátka, lektinová dráha je zahájena vazbou sérového lektinu MBL na sacharidové struktury na povrchu mikrobů a alternativní dráha je aktivována dalšími strukturami na povrchu mikrobů. Aktivace všech tří drah vede k tvorbě membranolytického komplexu (membrane attack complex, MAC), který vyvolává osmotickou lýzu buněk (Obr. 6). Aktivace jednotlivých složek vede ke vzniku dvou fragmentů – fragment b (např. C3b) je obvykle větší a dále se účastní komplementové kaskády, zatímco menší fragment a (např. C3a), označovaný jako anafylatoxin, má jinou biologickou aktivitu. Anafylatoxiny (C3a, C4a a C5a) způsobují silnou kontrakci hladkosvalových vláken a zvyšují vaskulární permeabilitu. Nejúčinnějším anafylatoxinem je C5a, který je extrémně silný stimulant chemotaxe, adherence, respiračního vzplanutí a degranulace neutrofilů. Po vazbě na C5a receptor vyvolává mobilizaci arachidonátu a jeho přeměnu na prostaglandiny a leukotrieny v neutrofilech, zatímco v monocytech indukuje uvolnění interleukinu-1 (IL-1). Fragmenty C3b a C4b a rovněž lektin MBL účinkují jako opsoniny, které se váží na povrch mikrobů, označují je a usnadňují jejich fagocytózu. Opsoniny tedy podporují a zesilují fagocytózu.
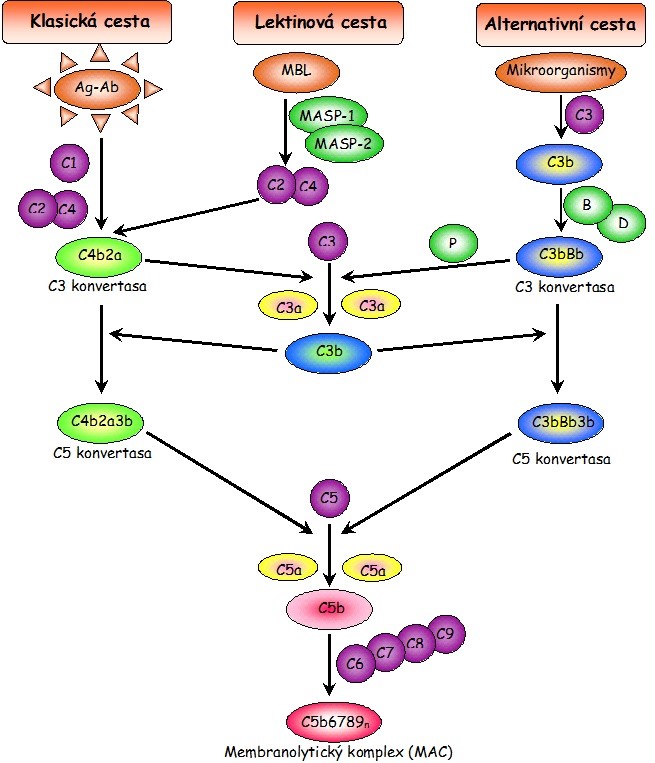
Obr. 6. Aktivace jednotlivých drah komplementu
Cytokiny
Cytokiny jsou vysoce aktivní signální sloučeniny proteinové povahy s krátkým biologickým poločasem, které vykazují autokrinní a parakrinní účinky. Po vazbě na specifický receptor regulují buněčné funkce organismu. Jsou syntetizovány, skladovány a transportovány různými typy buněk nejen imunitního systému (lymfokiny, interleukiny, monokiny, tumor-nekrotizující faktory, interferony), ale i dalších buněk studovaných v hematologii (kolonie-stimulující faktory), onkologii (transformující růstové faktory) a buněčné biologii (peptidové růstové faktory, stresové proteiny). Cytokiny kontrolují směr, rozsah a trvání imunitní odpovědi a kontrolují remodelaci tkání. Mezi charakteristické rysy většiny cytokinů patří, že působí na několik různých typů buněk (jsou pleiotropní), účinek cytokinu je pro něj typický (specifita), jeden cytokin indukuje tvorbu druhého (působí v kaskádě) a jednotlivé cytokiny mohou být nahrazeny jinými (určitá míra redundance cytokinového systému). Účinky různých cytokinů se vzájemně doplňují (synergismus), nebo jeden cytokin blokuje účinky jiného (antagonismus). S ohledem na zánět rozlišujeme dvě hlavní skupiny cytokinů – prozánětlivé a protizánětlivé. Prozánětlivé cytokiny (IL-1, IL-6, IL-8 a tumor-nekrotizující faktor-α (TNF-α)) jsou syntetizované hlavně aktivovanými makrofágy a stimulují zánětlivé reakce. Navozují změny v místě zánětlivého postižení - stimulují antigen prezentující a endotelové buňky k expresi adhezních molekul. Výsledkem je aktivace, diferenciace a proliferace zánětlivých buněk. IL-8 jako chemoatraktant pro neutrofily. Ústřední úlohu v zánětlivé odpovědi mají IL-1 a TNF, které působí také systémově a navozují reakci akutní fáze včetně ovlivnění syntézy proteinů v játrech (proteiny akutní fáze) a vzniku horečky (spolu s IL-6). Protizánětlivé cytokiny (IL-4, IL-10 a IL-13) jsou produkovány T-lymfocyty, tlumí zánětlivou odpověď a inhibují produkci prozánětlivých cytokinů.
Exogenní mediátory zánětu
Rozpoznání patogenních mikroorganismů imunitním systémem je umožněno díky přítomnosti specifických molekul/molekulárních vzorů („pathogen associated molecular patterns“, PAMP), které jsou fylogeneticky značně zakonzervované. Jejich nositeli jsou pouze mikroorganismy a pro přežití daného mikroorganismu jsou esenciální. Patří mezi ně např. složky bakteriální stěny (lipopolysacharid Gram¯ bakterií = endotoxin, peptidoglykany, flagelin, lipoteichoová kyselina), bakteriální DNA (mnoho C a G, bez methylace) a virová dsRNA, N-formylmethionylpeptidy (FMLP, pouze bakterie využívají formylovaný methionin k syntéze proteinů), fungální β-glukany a chitin. Molekuly PAMP jsou rozeznávány PRR receptory („pattern recognition receptors“) a aktivují mechanismy vrozené imunity. PRR receptory jsou přítomné na membránách všech buněk těla, zejména pak buněk přirozené imunity (Toll-like receptory, C-lektinové receptory, scavengerové receptory, imunoglobulinové receptory), ale i v nitrobuněčných strukturách (NOD-like receptory, receptory NLRP, RIG-like receptory) a v tělních tekutinách (pentraxiny, kolektiny, fikoliny).