Antioxidační systém organismu
Antioxidační obrana organismu představuje komplexní systém tvořený několika úrovněmi. Podle vztahu k tvorbě ROS lze tyto obranné mechanismy rozdělit do tří skupin. Primární antioxidanty brání tvorbě volných radikálů (např. chelátory iontů, inhibitory xanthinoxidasy a NADPH-oxidasy, transportní bílkoviny), sekundární vychytávají již vytvořené volné radikály (např. antioxidační enzymy a redukující látky) a terciární zajišťují opravu a eliminaci biomolekul poškozených volnými radikály (např. methioninsulfoxidreduktasa, DNA-fotolyasa, fosfolipasy, proteasy, endonukleasy). Ochrana organismu proti oxidačnímu poškození je systémem, v němž antioxidanty a celá jejich seskupení vzájemně spolupracují. Funkce jednoho antioxidantu velmi často podmiňuje účinek jiného článku tohoto systému.
Antioxidační enzymy
Mezi hlavní antioxidační enzymy organismu patří superoxiddismutasa (SOD), katalasa (CAT), glutathionperoxidasa (GPx) a další peroxidasy (Obr. 3).
Superoxiddismutasa, která je přítomná v každé aerobní buňce, katalyzuje dismutaci O2ˉ• na H2O2 a O2. U člověka se vyskytují tři formy enzymu – Cu,Zn-SOD, EC-SOD a Mn-SOD, které se liší kofaktorem (atom kovu) a lokalizací. Cu,Zn-SOD je přítomná v cytoplasmě buněk. Jedná se o homodimer, jehož každá podjednotka obsahuje po jednom atomu Cu a Zn; měď přenáší elektron z jedné molekuly superoxidu na druhou, zatímco zinek má stabilizační funkci a katalýzy se neúčastní. EC-SOD (extracelulární) je tetramer obsahující v aktivním místě ionty Cu a Zn. Tento enzym se váže prostřednictvím heparansulfátu na luminální povrchu endotelu, odkud může být uvolněn heparinem. Mn-SOD je lokalizována v matrix mitochondrií a má čtyři podjednotky; spolu s Fe-SOD se vyskytuje i v prokaryontních organismech a je tedy fylogeneticky starší než Cu,Zn-SOD. U člověka vede deficit Cu,Zn-SOD k onemocnění zvanému amyotrofická laterální sklerosa, které je provázeno těžkým postižením motorických neuronů v mozkové kůře a míše.
Peroxid vodíku, který vzniká dismutací O2ˉ•, je toxický, proto se ho organismus snaží co nejrychleji odstranit. K tomuto účelu se vyvinuly dva systémy – katalasa (štěpí H2O2 na H2O a O2) a peroxidasy (redukce H2O2 je provázena oxidací jiného substrátu). U člověka je nejvýznamnější peroxidasou glutathionperoxidasa, která redukuje H2O2 za současné oxidace glutathionu (GSH). Regeneraci koenzymu GSH zajišťuje glutathionreduktasa (GR), která využívá k redukci oxidovaného glutathionu (GSSG) koenzym NADPH. Je tedy závislá na správném fungování pentosového cyklu. U člověka bylo popsáno osm isoenzymů GPx, které se liší strukturou, lokalizací, funkcí a závislostí na selenu. GPx1 se nachází v cytoplasmě prakticky všech buněk (cGPx) a kromě antioxidační úlohy slouží zřejmě i jako zásobárna selenu; GPx2 (GIT) a GPx3 (plasma) jsou lokalizovány extracelulárně. Všechny tři isoformy mají podobnou tetramerní strukturu a obsahují v aktivním centru selenocystein, který slouží jako redoxní centrum enzymu. GPx4 (též fosfolipidová GPx, PHGPx), zřejmě nejvýznamnější antioxidačně působící isoforma, je monomerní enzym vázaný v buněčných membránách všech buněk, kde redukuje kromě H2O2 i lipidové hydroperoxidy. GPx5 je hlavním enzymem v nadvarleti, který má tetramerní strukturu a v aktivním centru má cysteinový zbytek místo slenocysteinu. GPx6 je strukturně blízká GPx3 (homotetramer se selenocysteinem), ale její funkce a kinetické vlastnosti jsou předmětem dalšího studia. GPx7 a GPx8 jsou monomerní enzymy, v nichž je selenocystein nahrazen redoxně aktivním cysteinovým zbytkem. Tyto enzymy jsou lokalizovány v membránách endoplasmatického retikula a podílejí se na skládání nascentních proteinů. Dědičný defekt GPx a defekt tvorby GR se projeví poškozením buněčných membrán s následnou hemolytickou anemií.
Katalasa působí na H2O2 až ve vysokých koncentracích, čímž se liší od peroxidas, které působí na nízké koncentrace H2O2. CAT může katalyzovat i peroxidasové reakce, ale vzhledem k nízké aktivitě vůči alkylperoxidům (ROOH) se tato reakce v antioxidační obraně neuplatňuje. Jedná se o hemoprotein se čtyřmi podjednotkami, který vykazuje nejvyšší aktivitu v mitochondriích a peroxisomech hepatocytů a v cytoplasmě erythrocytů. Dědičný deficit CAT je velmi vzácný a nemá závažné klinické projevy.
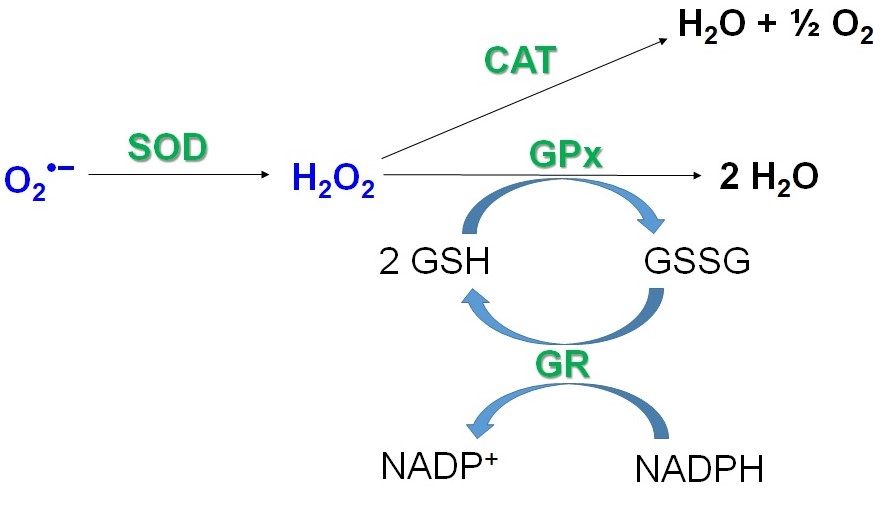
Obr. 3. Vztahy mezi jednotlivými součástmi antioxidačního systému buňky (upraveno z Racek 2003).
Vysokomolekulární endogenní antioxidanty
Přechodné kovy (zejm. železo a měď) se chovají jako volné radikály a jsou-li volné a v redukované formě podílejí se na vzniku ROS (účastní se Fentonovy reakce). Organismus potřebuje Fe a Cu jako biogenní stopové prvky, musí však zabránit jejich účasti v radikálových reakcích. Ochranou před účastí těchto kovů ve Fentonově reakci je jejich vazba v pevném chelátu (např. transportní a skladovací proteiny) nebo oxidace na vyšší valenci. Tak je Fe(III) při transportu v plasmě pevně vázáno na transferin. V buňkách střevní sliznice a v kostní dřeni je pevně vázáno v molekule feritinu, v leukocytech se váže na protein laktoferin. Železo se sice vstřebává jako dvoumocné, avšak feritin vykazuje ferooxidasovou aktivitu, která udržuje skladované Fe v oxidované formě. Stejně tak v krvi zajišťuje oxidaci železa ceruloplasmin, jehož hlavním funkcí není transport Cu, ale právě oxidace Fe před jeho předáním transferinu. Za antioxidant můžeme považovat i haptoglobin (vychytává extracelulární hemoglobin) a hemopexin (váže uvolněný hem), protože uvolněný hemoglobin a hem představují prooxidačně nebezpečnou formu Fe. Reaktivitu volných radikálů významně ovlivňují také thiolové skupiny některých proteinů (např. albumin, metalothioneiny), které chelatují ionty kovů.
Nízkomolekulární antioxidanty
Antioxidant můžeme definovat jako sloučeninu, která – je-li přítomná v nízkých koncentracích v porovnání s množstvím oxidovatelného substrátu – je schopná jeho oxidaci značně zpomalit nebo jí zabránit. Podle upravené definice, která je vhodná pouze pro nízkomolekulární antioxidanty, by „ideální“ antioxidant měl být: netoxický; vstřebáván z potravy a dostupný po absorpci; přeměněn v buňkách a tkáních na redukovanou formu, aby mohl vystupovat jako donor protonů nebo elektronů; schopen zničit volné radikály a vykazovat řadu antioxidačních vlastností včetně interakce s dalšími antioxidanty přítomnými v membráně nebo ve vodné fázi.
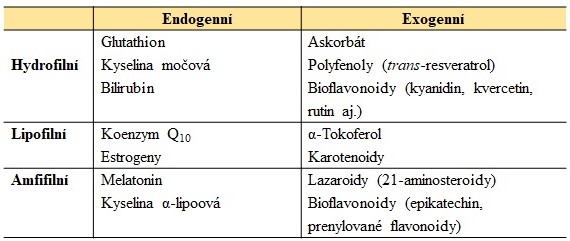
Nízkomolekulární antioxidanty můžeme dělit podle jejich původu (endogenní x exogenní; přirozené x umělé), lokalizace (intracelulární x extracelulární) či rozpustnosti (hydrofilní x lipofilní x amfifilní). Přehled nízkomolekulárních antioxidantů je uveden v Tab. 3.
Tab. 3. Přehled nízkomolekulárních antioxidantů