Hlavní biochemické mechanismy buněčného poškození
Hlavními biochemickými mediátory buněčného poškození jsou deplece ATP, poškození mitochondrií, influx kalcia a porušení kalciové homeostázy, nahromadění reaktivních forem kyslíku (ROS), defekty v membránové permeabilitě, poškození DNA a proteinů (Obr. 4).
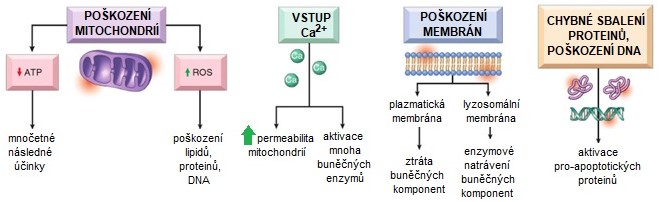
Obr. 4. Hlavní biochemické mechanismy buněčného poškození (upraveno z Kumar a kol. 2014).
Deplece ATP
Základní příčinou buněčné nekrózy je pokles hladin ATP. Deplece ATP a pokles syntézy ATP jsou obvykle vyvolány nedostatečným přívodem kyslíku a živin (hypoxie/ischemie), poškozením mitochondrií a účinkem některých chemických škodlivin (např. kyanidu). Energie ve formě ATP je vyžadována většinou syntetických i degradačních procesů v buňce (membránový transport, lipogeneze, proteosyntéza, deacylace-reacylace membránových fosfolipidů). Pokles koncentrace ATP na 5-10 % normální koncentrace má dopad na mnoho klíčových buněčných procesů. To vše výrazně ovlivňuje integritu plasmatické membrány, jejíž porucha je jednou z hlavních příčin zániku buňky.
Poškození mitochondrií
Mitochondrie hrají klíčovou úlohu ve všech typech buněčného poškození a smrti. K poškození mitochondrií dochází působením intracelulárního Ca2+, ROS či nedostatkem kyslíku, takže jsou citlivé k prakticky všem typům poškození včetně hypoxie/ischemie a chemických škodlivin. Mutace v mitochondriální DNA jsou příčinou vzniku některých vrozených onemocnění. Následkem poškození mitochondrií dochází k otevření mitochondriálních kanálů MPTP („mitochondrial permeability transition pore“) a následné ztrátě membránového potenciálu, útlumu oxidační fosforylace a progresivní depleci ATP. Změny v oxidační fosforylaci způsobují vznik ROS. Ztráta integrity mitochondriálních membrán způsobí uvolnění cytochromu c do cytosolu a následnou aktivaci prokaspas, který zpouští apoptózu.
Influx Ca2+ a narušení kalciové homeostázy
Rozdíl mezi koncentracemi Ca uvnitř buňky (0,1 µM) a v extracelulárním prostoru (1,3 mM) přesahuje 4 řády. Tento koncentrační gradient, který je podmínkou životaschopnosti buňky, je umožněn sekvestrací intracelulárního Ca2+ do mitochondrií a ER a do extracelulárního prostoru působením Ca/Mg-ATPasy. Některé toxiny a ischemie způsobují rychlý nárůst cytosolového Ca2+ tokem z ER a mitochondrií a později influxem z extracelulárního prostoru a vyvolají tak nespecifické zvýšení membránové permeability a aktivaci řady enzymů poškozujících buněčné struktury (fosfolipasy, proteasy, ATPasy, endonukleasy). Vysoké hladiny intracelulárního Ca2+ spouštějí apoptózu jednak přímou aktivací kaspas a také zvýšením permeability mitochondrií. Nahromadění Ca2+ v mitochondriích způsobí otevření membránového póru MPTP a následné selhání syntézy ATP (Obr. 5).
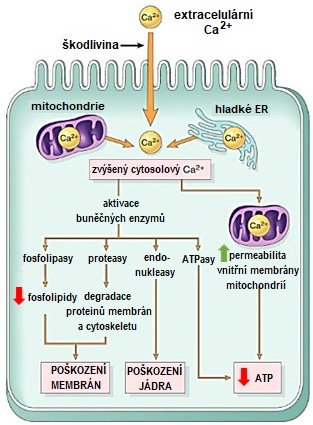
Obr. 5. Účast zvýšeného intracelulárního kalcia v buněčném poškození (upraveno z Kumar a kol. 2014).
Nahromadění ROS (oxidační stres)
Reaktivní formy kyslíku jsou mediátory buněčné smrti u řady patologických stavů. Způsobují peroxidaci lipidových komponent buňky, oxidaci proteinů a DNA, což má nepříznivý dopad na buněčné struktury (Obr. 6). Podrobnější informace jsou uvedeny v kapitole 2.
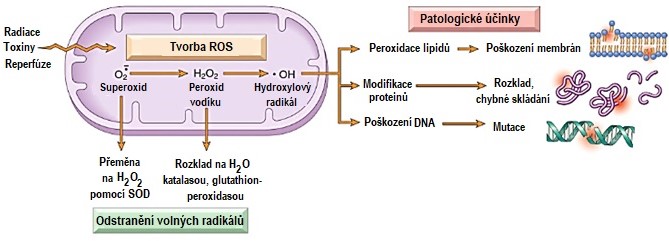
Obr. 6. Vznik, odstranění a úloha ROS v buněčném poškození (upraveno z Kumar a kol. 2014).
Defekty v membránové permeabilitě
Jednou z počátečních fází poškození buňky je ztráta selektivní membránové permeability, která nakonec vede ke zjevnému poškození membrány, je společným rysem prakticky všech forem poškození buňky. Membránové defekty jsou výlsedkem řady událostí, jako je deplece ATP či aktivace fosfolipas zvýšenou hladinou intracelulárního Ca2+. Některé bakteriální toxiny, virové proteiny, lytické složky komplementu, perforin lymfocytů a řada fyzikálních a chemických agens způsobuje přímé poškození plasmatické membrány. K poškození membrány mohou přispět i některé biochemické mechanismy (Obr. 7).
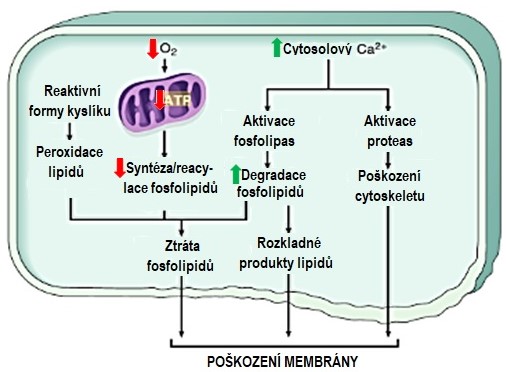
Obr. 7. Mechanismy poškození membrány v buněčném poškození (upraveno z Kumar a kol. 2014).
Poškození DNA a proteinů
Buňky sice disponují reparačními mechanismy pro opravu poškozené DNA, ale pokud je poškození příliš rozsáhlé (např. po vystavení DNA radiaci, oxidačnímu stresu nebo některým xenobiotikům), zahájí buňka sebevražedný program, který vede ke smrti buňky apoptózou. Podobnou reakci nastartují i chybně složené proteiny, které mohou vzniknout následkem dědičné mutace nebo působením volných radikálů.